Регуляция кроветворения: механизмы и важные факторы
Содержание:
- Постэмбриональный гемопоэз
- Филиалы и отделения Центра, в которых лечат злокачественные заболевания кроветворной системы
- Кроветворение в антенатальном периоде
- Заболевания крови
- Васкуляризация. Иннервация. Возрастные изменения. Регенерация.
- Регуляция гемопоэза
- ГЛАВА 10 КЛИНИЧЕСКАЯ ТАКТИКА ПРИ ВЕНОЗНЫХ ТРОМБОЗАХ
- Профилактика заболеваний крови
- ГЛАВА 4 МАКРОЦИТОЗ И МЕГАЛОБЛАСТНАЯ АНЕМИЯ
- Цитогенетический метод исследования крови
Постэмбриональный гемопоэз
Постэмбриональный гемопоэз представляет собой процесс физиологической регенерации крови, который компенсирует физиологическое разрушение дифференцированных клеток. Он подразделяется на миелопоэз и лимфопоэз.
Миелопоэз происходит в миелоидной ткани, расположенной в эпифизах трубчатых и полостях многих губчатых костей. Здесь развиваются эритроциты, гранулоциты, моноциты, тромбоциты, а также предшественники лимфоцитов. В миелоидной ткани находятся стволовые клетки крови и соединительной ткани. Предшественники лимфоцитов постепенно мигрируют и заселяют тимус, селезенку, лимфоузлы и некоторые другие органы.
Лимфопоэз происходит в лимфоидной ткани, которая имеет несколько разновидностей, представленных в тимусе, селезенке, лимфоузлах. Она выполняет функции образования T- и B-лимфоцитов и иммуноцитов (например, плазмоцитов).
Миелоидная и лимфоидная ткани являются разновидностями соединительной ткани, т.е. относятся к тканям внутренней среды. В них представлены две основные клеточные линии — клетки ретикулярной ткани и гемопоэтические клетки.
Ретикулярные, а также жировые, тучные и остеогенные клетки вместе с межклеточным веществом формируют микроокружение для гемопоэтических элементов. Структуры микроокружения и гемопоэтические клетки функционируют в неразрывной связи друг с другом. Микроокружение оказывает воздействие на дифференцировку клеток крови (при контакте с их рецепторами или путем выделения специфических факторов).
Таким образом, для миелоидной и всех разновидностей лимфоидной ткани характерно наличие стромальных и гемопоэтических элементов, образующих единое функциональное целое.
СКК относятся к самоподдерживающейся популяции клеток. Они редко делятся. Выявление СКК стало возможным при применении метода образования клеточных колоний – потомков одной стволовой клетки.
Пролиферативную активность СКК регулируют колониестимулирующие факторы (КСФ), различные виды интерлейкинов (ИЛ-3 и др.).
Каждая СКК в эксперименте или лабораторном исследовании образует одну колонию и называется колониеобразующей единицей (сокращенно КОЕ, CFU).
Исследование клеточного состава колоний позволило выявить две линии их дифференцировки.
Одна линия дает начало мультипотентной клетке — родоначальнице гранулоцитарного, эритроцитарного, моноцитарного и мегакариоцитарного рядов гемопоэза (сокращенно КОЕ-ГЭММ).
Вторая линия дает начало мультипотентной клетке — родоначальнице лимфопоэза (КОЕ-Л).
Из мультипотентных клеток дифференцируются олигопотентные (КОЕ-ГМ) и унипотентные родоначальные клетки.
Методом колониеобразования определены родоначальные унипотентные клетки для моноцитов (КОЕ-М), нейтрофильных гранулоцитов (КОЕ-Гн), эозинофилов (КОЕ-Эо), базофилов (КОЕ-Б), эритроцитов (БОЕ-Э и КОЕ-Э), мегакариоцитов (КОЕ-МГЦ), из которых образуются клетки-предшественники. В лимфопоэтическом ряду выделяют унипотентные клетки — предшественницы для B-лимфоцитов и для T-лимфоцитов. Полипотентные (плюрипотентные и мультипотентные), олигопотентные и унипотентные клетки морфологически не различаются.
Все приведенные выше стадии развития клеток составляют четыре основных класса, или компартмента, гемопоэза:
- I класс — СКК — стволовые клетки крови (плюрипотентные, полипотентные);
- II класс — КОЕ-ГЭММ и КОЕ-Л — коммитированные мультипотентные клетки (миелопоэза или лимфопоэза);
- III класс — КОЕ-М, КОЕ-Б и т.д. — коммитированные олигопотентные и унипотентные клетки;
- IV класс — клетки-предшественники (бласты, напр.: эритробласт, мегакариобласт и т.д.).
Сразу отметим, что оставшиеся два класса гемопоэза составляют созревающие клетки (V класс) и зрелые клетки крови (VI класс).
Эритропоэз у млекопитающих и человека протекает в костном мозге в особых морфофункциональных ассоциациях, получивших название эритробластических островков.
Эритробластический островок состоит из макрофага, окруженного одним или несколькими кольцами эритроидных клеток, развивающихся из унипотентной КОЕ-Э, вступившей в контакт с макрофагом. КОЕ-Э и образующиеся из нее клетки (от проэритробласта до ретикулоцита) удерживаются в контакте с макрофагом его рецепторами.
У взрослого организма потребность в эритроцитах обычно обеспечивается за счет усиленного размножения эритробластов. Но всякий раз, когда потребность организма в эритроцитах возрастает (например, при потере крови), эритробласты начинают развиваться из предшественников, а последние — из стволовых клеток.
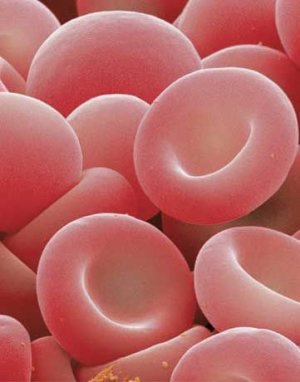
В норме из костного мозга в кровь поступают только эритроциты и ретикулоциты.
Филиалы и отделения Центра, в которых лечат злокачественные заболевания кроветворной системы
ФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, химиотерапевтического и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.
Отдел лекарственного лечения злокачественных новообразований МРНЦ имени А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России
Заведующая отделом, д.м.н. ФАЛАЛЕЕВА Наталья Александровна
8 (484) 399 – 31-30, г. Обнинск, Калужской области
Отдел лекарственного лечения опухолей МНИОИ имени П.А. Герцена –филиал ФГБУ «НМИЦ радиологии» Минздрава России
Заведующий отделом, д.м.н. ФЕДЕНКО Александр Александрович
8 (494) 150 11 22
Кроветворение в антенатальном периоде
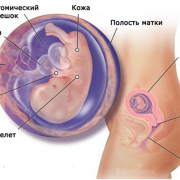
Кроветворение в антенатальном периоде впервые обнаруживается у 19-дневного эмбриона в кровяных островках желточного мешка, в стебле и хорионе. К 22-му дню первые кровяные клетки проникают в мезодермальную ткань эмбриона, в сердце, аорту, артерии. На 6-й нед. снижается активность К. в желточном мешке. Полностью первый (мезобластический) период гемопоэза, преимущественно эритроцитопоэза, заканчивается к началу 4-го мес. жизни эмбриона. Примитивные кроветворные клетки желточного мешка накапливают гемоглобин и превращаются в примитивные эритробласты, названные П. Эрлихом мегалобластами.
Второй (печеночный) период К. начинается после б нед. и достигает максимума к 5-му мес. К. этого периода преимущественно эритроидное, хотя на 9-й нед. в печени уже созревают первые нейтрофилы. Печеночный период эритроцитопоэза характеризуется исчезновением мегалобластов; при этом эритрокариоциты имеют нормальные размеры. На 3-м мес. эмбриональной жизни в эритроцитопоэз включается селезенка, но у человека ее роль в пренатальном К. ограничена.
На 4—5-м мес. начинается третий (костномозговой) период К. Миелоидный эритроцитопоэз плода — эритробластический и, как и лейкоцитопоэз, мало отличается от эритроцитопоэза взрослого.
Общей закономерностью эмбрионального эритроцитопоэза является постепенное уменьшение размеров эритроцитов и увеличение их числа. Соответственно различным периодам К. (мезобластическому, печеночному и костномозговому) существует три разных типа гемоглобина: эмбриональный, фетальный и гемоглобин взрослого. В основном переход от фетального гемоглобина к гемоглобину взрослого начинается на 3-й нед. жизни плода и заканчивается через 6 мес. после рождения.
В первые дни у новорожденных наблюдается полиглобулия и нейтрофильный лейкоцитоз. Затем активность эритроцитопоэза снижается. Нормализуется он в возрасте 2—3 мес. Нейтрофилез первых дней жизни сменяется лимфоцитозом; только к 5 годам в лейкоцитарной формуле начинают преобладать нейтрофилы.
Заболевания крови
Под общим понятием анемии, которую фиксирует медкнижка, подразумевается группа заболеваний, обусловленных пониженным уровнем гемоглобина. Деление на разновидности происходит на основании причин, вызвавших нарушение состава крови. Гемолитические анемии, вызванные генетическими наследственными дефектами, лечению не поддаются. Приобретенные гемолитические анемии вызваны чаще всего вредным воздействием различных факторов окружающей среды, а потому излечимы.
Онкологические болезни крови (гемобластозы), которые периодический профосмотр не выявит, подразделяют на два вида. При лейкозах начинается поражение костного мозга, что приводит к изменению структуры крови. При лимфомах нарушаются функции и строение лимфоцитов, а изменения строения костного мозга начинаются на финальной стадии заболевания.
Нарушения свертываемости крови классифицируют в зависимости от того, какие клеточные структуры или процессы свертывающей системы крови дали сбой. Исходя из специфики нарушений в составе крови, кроме данных видов, выделяют еще и другие варианты патологий.
Диагностика заболеваний крови возможна на уровне простых анализов, просто сделать УЗИ и получить ответ не получится. Болезни крови могут иметь вирусное, инфекционное, наследственное или хроническое происхождение. К аутоиммунным болезням относятся те, при которых иммунная система начинает уничтожать собственные клетки.
Терапия заболеваний крови включает целый комплекс мер по обеспечению восстановления функций системы кроветворения. Терапевтические методы отличаются для каждого вида заболеваний.
Васкуляризация. Иннервация. Возрастные изменения. Регенерация.
Васкуляризация. Костный мозг снабжается кровью посредством сосудов, проникающих через надкостницу в специальные отверстия в компактном веществе кости. Войдя в костный мозг, артерии разветвляются на восходящую и нисходящую ветви, от которых радиально отходят артериолы. Сначала они переходят в узкие капилляры (2—4 мкм), а затем в области эндоста продолжаются в широкие тонкостенные с щелевидными порами синусы (диаметром 10—14 мкм). Из синусов кровь собирается в центральную венулу. Постоянное зияние синусов и наличие щелей в эндотелиальном пласте обусловливаются тем, что в синусах гидростатическое давление несколько повышено, так как диаметр выносящей вены меньше по сравнению с диаметром артерии. К базальной мембране с наружной стороны прилежат адвентициальные клетки, которые, однако, не образуют сплошного слоя, что создает благоприятные условия для миграции клеток костного мозга в кровь. Меньшая часть крови проходит со стороны периоста в каналы остеонов, а затем в эндост и синус. По мере контакта с костной тканью кровь обогащается минеральными солями и регуляторами кроветворения.
Кровеносные сосуды составляют половину (50%) массы костного мозга, из них 30% приходится на синусы. В костном мозге разных костей человека артерии имеют толстую среднюю и адвентициальную оболочки, многочисленные тонкостенные вены, причем артерии и вены редко идут вместе, чаще врозь.
Капилляры бывают двух типов: узкие 6—20 мкм и широкие синусоидные (или синусы) диаметром 200—500 мкм. Узкие капилляры выполняют трофическую функцию, широкие являются местом дозревания эритроцитов и выхода в кровоток разных клеток крови. Капилляры выстланы эндотелиоцитами, лежащими на прерывистой базальной мембране.
Иннервация. В иннервации участвуют нервы сосудистых сплетений, нервы мышц и специальные нервные проводники к костному мозгу. Нервы проникают в костный мозг вместе с кровеносными сосудами через костные каналы. Далее покидают их и продолжаются как самостоятельные веточки в паренхиме в пределах ячеек губчатого вещества кости. Они ветвятся на тонкие волоконца, которые либо вновь вступают в контакт с костномозговыми сосудами и оканчиваются на их стенках, либо заканчиваются свободно среди клеток костного мозга.
Возрастные изменения. Красный костный мозг в детском возрасте заполняет эпифизы и диафизы трубчатых костей и находится в губчатом веществе плоских костей. Примерно в 12—18 лет красный костный мозг в диафизах замещается желтым. В старческом возрасте костный мозг (желтый и красный) приобретает слизистую консистенцию и тогда называется желатинозным костным мозгом. Следует отметить, что этот вид костного мозга может встречаться и в более раннем возрасте, например при развитии костей черепа и лица.
Регенерация. Красный костный мозг обладает высокой физиологической и репаративной регенерационной способностью. Источником образования гемопоэтических клеток являются стволовые клетки, находящиеся в тесном взаимодействии с ретикулярной стромальной тканью. Скорость регенерации костного мозга в значительной мере связана с микроокружением и специальными ростстимулирующими факторами гемопоэза.
Некоторые термины из практической медицины:
- миелограмма (миело- + греч. gramma запись) — выраженный в форме таблицы или диаграммы результат микроскопии мазка пунктата костного мозга, отражающий качественный и количественный состав ядросодержащих клеток миелоидной ткани.;
- миелоидная реакция (миело- + греч. —eides подобный) — появление в периферической крови малодифференцированных клеток, относящихся к грануло- и эритропоэтическому ряду; наблюдается при метастазах злокачественной опухоли в костный мозг, а также при сепсисе, туберкулезе и некоторых других болезнях;
- остеомиелит (osteomyelitis; остео- + греч. myelos костный мозг + ит; син.: костоеда — устар., паностит) — воспаление костного мозга, обычно распространяющееся на компактное и губчатое вещество кости и надкостницу;
| Часть первая – Общая характеристика, классификация; красный костный мозг | immunesys1.mp37 122 кБ |
| Часть вторая – Вилочковая железа — тимус | immunesys2.mp35 310 кБ |
| Часть третья – Селезенка | immunesys3.mp36 073 кБ |
| Часть четвертая – Лимфатические узлы, лимфоидная ткань слизистых оболочек | immunesys4.mp37 152 кБ |
Регуляция гемопоэза
Кроветворение регулируется:
- факторами роста, обеспечивающими пролиферацию и дифференцировку СКК и последующих стадий их развития,
- факторами транскрипции, влияющими на экспрессию генов, определяющих направление дифференцировки гемопоэтических клеток,
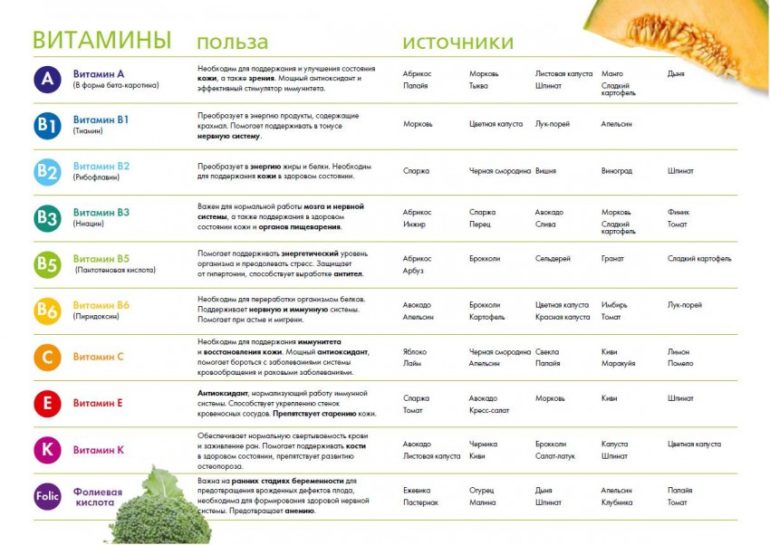
- витаминами, гормонами.
Факторы роста включают колониестимулирующие факторы (КСФ), интерлейкины и ингибирующие факторы. Они являются гликопротеинами, действующими и как циркулирующие гормоны, и как местные медиаторы, регулирующие гемопоэз и дифференцировку специфических типов клеток. Почти все факторы роста действуют на СКК, КОЕ, коммитированные и зрелые клетки. Однако отмечаются индивидуальные особенности действия этих факторов на клетки-мишени.
КСФ действуют на специфические клетки или группы клеток на различных стадиях дифференцировки. Например, фактор роста стволовых клеток влияет на пролиферацию и миграцию СКК в эмбриогенезе. В постнатальном периоде на гемопоэз оказывают влияние несколько КСФ, среди которых наиболее изучены факторы, стимулирующие развитие гранулоцитов и макрофагов (ГМ-КСФ, Г-КСФ, М-КСФ), а также интерлейкины.
Большинство указанных факторов выделено и применяется для лечения различных болезней. Для получения их используются биотехнологические методы.
Дифференцировка полипотентных клеток в унипотентные определяется действием ряда специфических факторов, поэтинов — эритропоэтинов (для эритробластов), гранулопоэтинов (для миелобластов), лимфопоэтинов (для лимфобластов), тромбопоэтинов (для мегакариобластов).
Большая часть эритропоэтина образуется в почках. Его образование регулируется содержанием в крови кислорода, которое зависит от количества циркулирующих в крови эритроцитов. Снижение числа эритроцитов и соответственно парциального давления кислорода, является сигналом для увеличения продукции эритропоэтина. Эритропоэтин действует на чувствительные к нему КОЕ-Э, стимулируя их пролиферацию и дифференцировку, что в конечном итоге приводит к повышению содержания в крови эритроцитов.
Тромбопоэтин синтезируется в печени, стимулирует пролиферацию КОЕ-МГЦ, их дифференцировку и образование тромбоцитов.
Ингибирующие факторы дают противоположный эффект, т.е. тормозят гемопоэз; их недостаток может быть одной из причин лейкемии, характеризующейся значительным увеличением числа лейкоцитов в крови. Выделен ингибирующий лейкемию фактор (ЛИФ), который тормозит пролиферацию и дифференцировку моноцитов-макрофагов.
Витамины необходимы для стимуляции пролиферации и дифференцировки гемопоэтических клеток. Витамин В12 поступает с пищей и соединяется с внутренним фактором (Касла), который синтезируется париетальными клетками желудка. Образуемый при этом комплекс, в присутствии ионов Са2+, соединяется с рецепторами эпителиоцитов подвздошной кишки и всасывается. При всасывании в эпителиоциты поступает лишь витамин В12, а внутренний фактор освобождается. Витамин В12 поступает с кровью в костный мозг, где влияет на гемопоэз, и в печень, где может депонироваться. Нарушение процесса всасывания при различных заболеваниях желудочно-кишечного тракта может служить причиной дефицита витамина В12 и нарушений в гемопоэзе.
Некоторые термины из практической медицины:
- анемия (син. малокровие) — состояние, характеризующееся снижением содержания гемоглобина в единице объема крови, чаще при одновременном уменьшении количества эритроцитов;
- анемия ахрестическая — общее название анемий, развивающихся вследствие неспособности эритробластов костного мозга использовать какие-либо антианемические факторы (цианокобаламин, фолиевую кислоту, железо и др.) при их нормальном поступлении в организм;
- хлороз ранний (син.: бледная немочь, хлороз ювенильный) — железодефицитная анемия у девушек в период полового созревания, проявляющаяся алебастровой бледностью кожи с зеленоватым оттенком, извращением вкуса, олигоменореей;
- хлороз поздний (син. анемия железодефицитная эссенциальная) — железодефицитная анемия у женщин в возрасте старше 30 лет, обычно связанная с маточными или другими кровотечениями, проявляющаяся извращением вкуса и обоняния, признаками атрофии слизистой оболочки полости рта и пищевода, выпадением волос, искривлением ногтей, позже — выраженными признаками анемии;
ГЛАВА 10 КЛИНИЧЕСКАЯ ТАКТИКА ПРИ ВЕНОЗНЫХ ТРОМБОЗАХ
Введение
Клиническая диагностика
Диагностика с помощью объективных методов
Практический подход к диагностике тромбоза глубоких вен
Рецедивы тромбоза глубоких вен
Подход к диагностике
Диагностика острого рецидива венозного тромбоза
Практический подход к диагностике острого рецидива венозного тромбоза
Диагностическая тактика в отношении больных с ранее нормальным результатом импедансной плетизмографии
Диагностическая тактика в отношении больных с аномальным или неизвестным результатом ранее проводившейся импедансной плетизмографии
Диагностика посттромбофлебитического синдрома
Другие причины болей в нижних конечностях
Субклинический тромбоз у больных, относящихся к группам высокого риска
Профилактика венозного тромбоза
Плановые абдоминальные и торакальные операции
Обширные операции на коленном суставе
Операции на органах мочеполовой системы
Инфаркт миокарда
Цереброваскулярные катастрофы
Диагностика тромбоэмболии легочной артерии
Сцинтиграфия сканирование легких
Ангиография легких
Рекомендуемый подход к диагностике тромбоэмболии легочной артерии
Тромбоз глубоких проксимальных вен и тромбоэмболия легочной артерии
Тромбоз глубоких вен голени
Тяжелая тромбоэмболия легочной артерии
Рецидив венозного тромбоза
Лечение посттромбофлебитического синдрома
Лечение тромбоневроза
Профилактика заболеваний крови
Профилактика патологий крови в первую очередь включает в себя ведение здорового образа жизни, что подтверждает также и водительская комиссия. Правильный и сбалансированный рацион питания, прием необходимых витаминов, профилактика переохлаждения и перегрева тела помогут избежать приобретенных заболеваний крови.
Кроме того, одной из важных мер предотвращения болезней крови является ограничение вредного воздействия на человека окружающей среды. Сюда можно отнести и вредное воздействие химических веществ, ионизирующее излучение, различные стрессовые ситуации.
Большую роль в профилактике играет забота о своем здоровье
Важно своевременно начинать лечение инфекционных заболеваний и паразитарных болезней, позаботиться о диагностике и терапии болезней, сопровождающихся кровотечениями
ГЛАВА 4 МАКРОЦИТОЗ И МЕГАЛОБЛАСТНАЯ АНЕМИЯ
Введение
Этиология
Для чего необходимо обследование
Ход обследования
Диагностика дефицита витамина В12
Диагностика дефицита фолиевой кислоты
Определение
Частота
Этиология
Клинические проявления
Диагностика
Лечение
Мегалобластная анемия после гастрэктомии
Распространенность
Этиология
Клинические проявления
Диагностика
Лечение
Мегалобластная анемия, обусловленная нарушением кишечной микрофлоры
Пищевой дефицит витамина В12
Пищевой дефицит фолиевой кислоты
Целиакия
Спру
Противосудорожные препараты
Бисептол
Хронические гемолитические состояния
Хронический миелофиброз
Переливание крови больным с тяжелой мегалобластной анемией
Цитогенетический метод исследования крови
в настоящее время входит в перечень необходимых диагностических мероприятий при большинстве онкогематологических заболеваний. Данный метод позволяет:
• Провести точную диагностику большинства опухолевых заболеваний системы крови.
• Определить прогноз заболевания.
• Использовать таргетную (точечную, прицельную терапию) при обнаружении определенных цитогенетических перестроек.
В основе развития онкогематологических заболеваний лежат перестройки (поломки) генетического материала в клетках кроветворной и лимфоидной тканей. Эти события приводят к трансформации нормальных кроветворных клеток в опухолевые. Они не затрагивают другие клетки организма (в т.ч. половые клетки). По этой причине онкогематологические заболевания, за редким исключением, не передаются по наследству. Хромосомные перестройки можно обнаружить при помощи стандартного цитогенетического исследования или более чувствительного метода – интерфазного анализа с использованием зондов (маркеров) к конкретным участкам хромосом (метод FISH). В ряде случаев цитогенетические изменения могут происходить на субмикроскопическом уровне (т.к называемые точечные мутации). Такие изменения возможно детектировать только с помощью ультратонких высокочувствительных методов молекулярного исследования (метод ПЦР- полимеразная цепная реакция).
Чем продиктована необходимость проведения молекулярно-цитогенетических исследований у онкогематологических больных? В настоящее время хорошо изучен ряд цитогенетических изменений, являющихся уникальными специфическими маркерами для различных вариантов опухолевых заболеваний системы крови. Их обнаружение является достоверным критерием диагноза. Яркими примерами могут служить транслокация t(9:22) или филадельфийская хромосома, присутствующая во всех случаях хронического миелолейкоза; транслокация t(15;17) — при остром промиелоцитарном лейкозе, транслокация t(8;14) – при лимфоме Беркитта. Кроме того, расшифровка цитогенетических событий привела к созданию таргетных препаратов, которые в отличие от химиопрепаратов обладают селективным действием на опухолевые клетки. Так, использование иматиниба при обнаружении филадельфийской хромосомы кардинально изменило прогноз хронического миелолейкоза.
В ходе больших международных исследований было обнаружено различное течение онкогематологических заболеваний в зависимости от обнаружения тех или иных хромосомных перестроек или мутаций генов. Известны изменения, ассоциированные с благоприятным, промежуточным или неблагоприятным агрессивным течением заболевания. Таким образом, молекулярно-цитогенетические характеристики являются предикторами прогноза. На этой основе при различных онкогематологических заболеваниях на ряду с другими признаками разрабатываются программы терапии разной интенсивности (риск-адаптированная терапия).
Среди опухолей кроветворной и лимфоидной тканей различают лимфомы и лейкозы. Исторически сложилось разделение лимфоидных опухолей (лимфом) на лимфому Ходжкина и неходжкинские лимфомы. Неходжкинские лимфомы в зависимости от клеточной линии подразделяются на В-клеточные, Т- и NK-клеточные опухоли. На сегодняшний день на основании морфоиммунологических и генетических характеристик выделяется несколько десятков видов неходжкинских лимфом, для многих из которых созданы обособленные терапевтические программы. Лейкозы представляют собой разнородную группу заболеваний, делятся на острые и хронические в зависимости от субстрата опухоли: при острых лейкозах основная масса клеточного субстрата представлена незрелыми клетками (бластами ), при этом блок дифференцировки происходит очень рано, на этапе клеток-родоначальниц кроветворения, в отличие от хронических лейкозов, где опухолевые клетки представлены зрелыми и созревающими элементами. Также принципиально важным является деление лейкозов на миелоидные и лимфоидные, что возможно только при проведении качественного морфо- цитохимического, иммунофенотипического и молекулярно-генетического исследований клеток крови еще до начала лечения.