Гемопоэз — классификация, физиология и механизмы регуляции образования клеток крови
Содержание:
- Лечение апластической анемии
- Наши врачи
- Кроветворение в антенатальном периоде
- Что будет, если гемопоэз нарушится
- Регуляция кроветворения
- Особенности дифференцировки гемопоэтических клеток
- Гемопоэтическая стволовая клетка
- Апластичная анемия: этиология
- Апластическая анемия: диагностика
- Основные этапы производства крови в организме
- Контроль гемоцитопоэза
- Регуляция гемопоэза
- Регуляция кроветворения
- Постэмбриональный гемопоэз
Лечение апластической анемии
Лечение идиопатической и других видов апластической анемии – очень сложная задача, требующая комплексного индивидуального подхода. При разработке тактики специалисты ЦЭЛТ учитывают результаты диагностики и показания пациента. Больного помещают в изолятор с асептическими условиями, что позволяет исключить риск развития инфекций и их осложнений. Медикаментозная терапия заключается в приёме:
- Глюкокортикоидов – при выявлении аутоиммунных механизмов и формировании антител против собственных кровяных клеток;
- Цитостатиков – при отсутствии эффекта от лечения глюкокортикоидами при аутоиммунной анемиии;
- Циклоспорина «А» – для подавления производства ФНО и интерферона “y”;
- Анаболиков – для стимулирования функции кроветворения;
- Андрогенов – для стимулирования образования красных кровяных клеток.
Всем больным апластической анемией проводят переливание эритроцитарной и/или тромбоцитарной массы, в объёмах, определяемых исходя из клинической картины и показателей периферической крови. Кроме того, пациенту могут назначить спленэктомию – хирургическое вмешательство, направленное на удаление селезёнки. Самые благоприятные прогнозы может обеспечить трансплантация костного мозга. Она заключается в пересадке донорских или собственных стволовых кроветворных клеток, предварительно изъятых из подвздошных костей путём пункции. К сожалению, процедура недоступна для широкого применения из-за сложности подбора совместимого донора. В том случае, если это невозможно, пациенту назначают паллиативную терапию с применение циклоспорина А.
В отделении гематологии нашей клиники ведут приём кандидаты, доктора и профессоры медицинских наук с опытом практической и научной работы от двадцати пяти лет. Вы можете записаться к ним на приём онлайн или обратившись к нашим операторам. Специалисты высокой квалификации работают и в отделении . К ним можно записаться на
В ЦЭЛТ вы можете получить консультацию гематолога.
- Первичная консультация — 3 200
- Повторная консультация — 2 000
Записаться на прием
Записавшись на прием гематолога, вы сможете получить всестороннюю консультацию. В компетенции врача находится лечение различных заболеваний крови, большинство из которых можно выявить на ранних стадиях и назначить своевременное лечение, позволяющее справиться с болезнью быстро и легко.
Наши врачи
Тюкалова Наталья Рудольфовна
Врач-гематолог, педиатр, кандидат медицинских наук
Стаж 29 лет
Записаться на прием
Дворецкий Леонид Иванович
Врач-терапевт, гематолог, доктор медицинских наук, профессор
Записаться на прием
Лабораторные исследования
- Клинический анализ крови — 950
руб. - Коагулограмма развернутая — 2 000
руб. - Обмен железа (железо несвязанное, трансферин) — 700
руб. - Витамин В 12 — 650
руб. - Фолиевая кислота — 650
руб. - Цитологическое исследование пунктатов (1 локализация) — 1 900
руб. - Цитологическое исследование пунктатов щитовидной железы и других органов и тканей (1 локализация) — 1 900
руб. - Гистологическое исследование биопсийного материала лимфоузлов — 3 500
руб. - Гистологическое исследование биопсийного материала ткани костного мозга — 4 500
руб.
- (печень, желчный пузырь, поджелудочная железа, селезенка) — 3 800 руб.
- УЗИ лимфатических узлов, комплексное (несколько регионов) — 3 000 руб.
- Ультразвуковое исследование и компрессионная поверхностных лимфатических узлов — 4 000 руб.
Рентгенологические исследования
Рентгенография органов грудной клетки (обзорная) — 2 500 руб.
Компьютерная и
- гепато-панкреато-дуоденальной области и селезенки — 11 000 руб.
- МР томография органов брюшной полости (печень, желчный пузырь, поджелудочная железа, селезенка) с внутривенным введением контрастного вещества — 14 000 руб.
Кроветворение в антенатальном периоде
Кроветворение в антенатальном периоде впервые обнаруживается у 19-дневного эмбриона в кровяных островках желточного мешка, в стебле и хорионе. К 22-му дню первые кровяные клетки проникают в мезодермальную ткань эмбриона, в сердце, аорту, артерии. На 6-й нед. снижается активность К. в желточном мешке. Полностью первый (мезобластический) период гемопоэза, преимущественно эритроцитопоэза, заканчивается к началу 4-го мес. жизни эмбриона. Примитивные кроветворные клетки желточного мешка накапливают гемоглобин и превращаются в примитивные эритробласты, названные П. Эрлихом мегалобластами.
Второй (печеночный) период К. начинается после б нед. и достигает максимума к 5-му мес. К. этого периода преимущественно эритроидное, хотя на 9-й нед. в печени уже созревают первые нейтрофилы. Печеночный период эритроцитопоэза характеризуется исчезновением мегалобластов; при этом эритрокариоциты имеют нормальные размеры. На 3-м мес. эмбриональной жизни в эритроцитопоэз включается селезенка, но у человека ее роль в пренатальном К. ограничена.
На 4—5-м мес. начинается третий (костномозговой) период К. Миелоидный эритроцитопоэз плода — эритробластический и, как и лейкоцитопоэз, мало отличается от эритроцитопоэза взрослого.
Общей закономерностью эмбрионального эритроцитопоэза является постепенное уменьшение размеров эритроцитов и увеличение их числа. Соответственно различным периодам К. (мезобластическому, печеночному и костномозговому) существует три разных типа гемоглобина: эмбриональный, фетальный и гемоглобин взрослого. В основном переход от фетального гемоглобина к гемоглобину взрослого начинается на 3-й нед. жизни плода и заканчивается через 6 мес. после рождения.
В первые дни у новорожденных наблюдается полиглобулия и нейтрофильный лейкоцитоз. Затем активность эритроцитопоэза снижается. Нормализуется он в возрасте 2—3 мес. Нейтрофилез первых дней жизни сменяется лимфоцитозом; только к 5 годам в лейкоцитарной формуле начинают преобладать нейтрофилы.
Что будет, если гемопоэз нарушится
К сожалению, встречаются заболевания, при которых нарушается одно или несколько звеньев производства крови. В зависимости от того, на каком уровне это произошло, тяжесть заболевания и его проявления будут варьировать.
Нарушение производства эритроцитов
Такое состояние возникает, если эритропоэз остановился до полного образования эритроцита. Основными проявлениями проблемы будут:
- снижение уровня гемоглобина в крови
- появление патологических форм гемоглобина
- повышенное разрушение недозрелых форм леток и, как
- следствие, появление желтухи
Нарушение производства лейкоцитов
Обычно такое нарушение связано с повышенной выработкой миелобластов или лимфоцитов, при этом развивается состояние знакомое всем как лейкоз. Клинически лейкоз появляется снижением общего иммунитета, присоединением множества инфекций и ненормальной реакцией организма на обычные процессы.
Нарушение производства тромбоцитов
Изменения в этом звене гемопоэза очень опасны, так как быстрее предыдущих ведут к гибели. Вся причина в том, что несовершенные тромбоциты не могут адекватно выполнить адгезивную функцию. Следовательно, даже малейшие повреждения будут сопровождаться массивными кровотечениями.
В заключении хочется сказать, что тонкие механизмы гемопоэза, практически не подвластны человеческому воздействию. Поэтому возникшие в них ошибки исправить бывает очень трудно.
Сен 29, 2016
Регуляция кроветворения
Регуляция кроветворения осуществляется посредством взаимодействия генетического потенциала с факторами окружающей среды, которые включают микросреду и факторы роста. Факторы роста, также называемые гемопоэтическими цитокинами, представляют собой семейство из более чем 20 гликопротеинов. Они продуцируются стромальными клетками, эндотелиальными клетками, фибробластами, макрофагами, лимфоцитами и другими. Некоторыми из наиболее известных гематопоэтических цитокинов являются гранулоцит-колониестимулирующий фактор, моноцит-колониестимулирующий фактор, эритропоэтин, тримбоцитопоэтин и другие. Их эффекты выражаются в стимулирующем или ингибирующем влиянии на деление, дифференцировку, пролиферацию и апоптоз клеток. Кроме того, они облегчают взаимодействие между стволовыми клетками и компонентами микроокружения.
Эритропоэтин – это гормон, который регулирует образование красных кровяных клеток. Вырабатывается в почках и в печени. Эритропоэтин действует путем связывания с рецепторами, расположенными на мембране эритроидных клеток. Эта связь между гормоном и рецептором стимулирует их дифференциацию и пролиферацию. Эритропоэтин действует на поздних стадиях эритропоэза.
Тромбоцитопоэтин – это гормон, который вырабатывается в печени на ранних стадиях кроветворения. В нормальных условиях большинство клеток костного мозга не делятся. Более зрелые клетки-предшественники пролиферируют и образуют относительно постоянное количество клеток крови, а некоторые из них подвергаются апоптозу. Этот тип кроветворения называют конститутивным, потому что это происходит в относительно постоянных условиях. Также различают индуцибельный гемопоэз, который стимулируется при наличии стресса в организме.
Кроветворение является жизненно важным процессом, подлежащим точной регуляции. Благодаря этому количество клеток крови в организме поддерживается относительно постоянным. Это позволяет крови выполнять свои важные физиологические функции.
Особенности дифференцировки гемопоэтических клеток
Кроветворная ткань костного мозга объединяет в своем составе комбинацию морфологически нераспознаваемых гемопоэтических клеток-предшественниц и клеток специфических рядов дифференцировки. Все кроветворные клетки, нераспознаваемые с точки зрения морфологии – это гемопоэтические стволовые клетки, которые могут быть:
- мультипотентными (дифференцируются во всех направлениях);
- полипотентными (развиваются только по некоторым из них);
- унипотентными (следуют только по определенному пути развития).
Другая часть клеток, которые удается распознать морфологически, формируется путем дифференцировки из более молодых предшественников, стремительно развивающихся дальше.
Миелопоэз может протекать в нескольких направлениях:
- мегакариоцитарное;
- эритроцитарное;
- моноцитарное;
- гранулоцитарное.
Лимфопоэз включает в себя две основные линии дифференцировки – образование лимфоцитов Т- и В-клеточного ряда. Каждая из них проходит в два этапа. Первый из них является антиген-независимым и заканчивается продукцией структурно зрелых, но иммунологически неактивных лимфоцитов. Следующий этап начинается после контакта с потенциальным антигеном и завершается выработкой специализированных иммунных клеток (Т-киллеров, Т-хелперов, Т-супрессоров, плазматических клеток, клеток памяти).
Каждый ряд дифференцировки кроветворных клеток дебютирует со стадии так называемых «бластов» (например, миелобласты). Для обозначения клеток промежуточного этапа используют приставку «про» и суффикс «цит» (например, проэритрокариоцит). Зрелые клеточные элементы имеют только суффикс «цит» (например, тромбоцит).
Следует отметить, что процесс дифференцировки различных видов клеточных элементов имеет свои особенности. Так, в гранулоцитарном ряде выделяют не одну, а несколько промежуточных стадий. В этом случае вслед за миелобластом образуется промиелоцит, затем миелоцит, метамиелоцит, а только после этого – зрелые клетки – эозинофилы, базофилы, нейтрофилы.
Гемопоэтическая стволовая клетка
Стволовые клетки обладают замечательным потенциалом дифференцироваться во многие различные типы клеток в организме. Кроме того, во многих тканях они служат своеобразной ремонтной средой. Стволовые клетки отличаются от других двумя важными характеристиками. Во-первых, они являются неспециализированными клетками и способны к регенерации путем деления клеток даже после длительных периодов бездействия. Во-вторых, при определенных условиях они могут быть вызваны определенными факторами, чтобы дифференцироваться в специфичные для органа клетки со специальными функциями.
Клетки крови образуются гемопоэтическими стволовыми клетками в результате процессов пролиферации и дифференцировки. Дифференциация регулируется факторами роста и цитокинами, которые выделяются клетками в микроокружении. После начала процессов дифференцировки гемопоэтические стволовые клетки теряют способность к самообновлению. Они могут дифференцироваться в клетки-предшественники, которые могут стать клетками крови в двух основных категориях: миелоидная линия или лимфоидная линия. После нескольких делений получают унипотентные клетки-предшественники, которые способны дифференцироваться только в одну клеточную линию – гранулоцит-моноцит, эритроид, мегакариоцит, B- или T-лимфоцит.
Апластичная анемия: этиология
Согласно происхождению, выделяют врождённую и приобретённую анемию. Первая развивается вследствие хромосомных мутаций, вторая – под воздействием химических веществ, излучения, инфекций. Специалисты считают, что угнетение кроветворения костного мозга может быть инициировано появлением в нём и в крови цитотоксических Т-лимфоцитов. Они производят ФНО (внеклеточный белок) и интерферон “y”, которые подавляюще воздействуют на ростки кроветворения. Причина запуска механизма может крыться в:
- Воздействии ионизирующего излучения или химических веществ в виде ароматических соединений, мышьяка, пестицидов;
- Попадании в организм инфекционных агентов (возбудители гепатитов “D”, “B”, цитомегаловируса, ДНК-содержащего вируса Эпштейна-Барр);
- Приёме миелотоксических препаратов при прохождении курса лечения транквилизаторами, противосудорожными, антитиреоидными и антиопухолевыми средствами;
- Развитии ряда аутоиммунных процессов (красная системная волчанка, поражение соединительной ткани – синдром Шегрена).
В 50% случаев причину развития патологии установить не удаётся. Такая форма апластической анемии называется идиопатической.
Апластическая анемия: диагностика
Перед тем, как приступить к лечению заболевания, гематологи ЦЭЛТ проводят комплексную диагностику, направленную на точную постановку диагноза и выявление этиологического фактора. Она включает в себя:
- осмотр у гематолога;
- общий и биохимический анализы крови;
- забор образца костного мозга и его исследование – стернальная пункция.
При наличии заболевания у пациента выявляют серьёзное снижение гемоглобина, вплоть до критического уровня – 20-30 г/л, наблюдается агранулоцитоз – снижение зернистых лейкоцитов и моноцитов. Количество лимфоцитов может быть в норме или сниженным, тромбоцитов – всегда снижено, иногда их не обнаруживают вовсе. Скорость оседания эритроцитов – повышается до 4-60 мм/ч. Исследование образца костного мозга выявляет повышенное содержание жировой ткани – 90%, включающее в себя элементы стромы и лимфы, а вот гематогенные клетки имеются в очень малом количестве.
Основные этапы производства крови в организме
Все этапы могут быть разделены по принципу того, какая клетка крови производится.
Производство эритроцитов
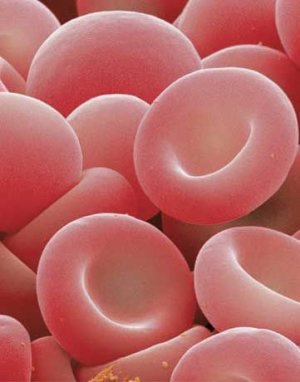
Эритроциты
Данный процесс осуществляется в 18 этапов. Самым первым этапом в дифференцировке является эритроцитарная единица (КОЕ-Э). Из нее развивается проэритробласт, который является самой первой клеткой предшественницей, которая самая первая находится в костном мозге. Через 5 делений проэритробласт теряет ядро и уже сам «плавает» в крови. Эритроцит живет около 120 дней.
Отработанные эритроциты редуцируются. При этом процесс равного разрушения и образования новых клеток должен строго контролироваться. Если у организма повышается нужда в эритроцитах, то их выработка ускоряется и наоборот.
В костном мозге может разрушаться часть эритроцитов. Нормальный уровень гемоглобина поддерживается в организме за счет гормонов и прочих веществ, оказывающих влияние на эритропоэз. Если вдруг клетка не завершила свое преобразование, процесс появления красных кровяных клеток считается неэффективным.
Производство лейкоцитов
Начальной единицей является миелобласт, после созревания которого происходят некоторые изменения. Ядро его уменьшается и миелобласт становится промиелоцитом. Такая клетка имеет маленькое ядро и уплотнения хроматина по периферии. Промиелоцит переходит в миелоцит.
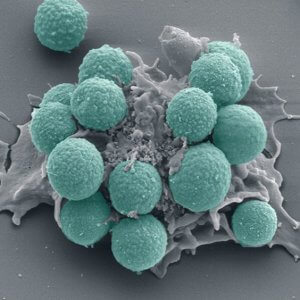
Лейкоциты
Миелоциты по предназначению делятся на базофильные, эозинофильные и нейтрофильные. Со временем они становятся метамиелоцитами, которые переходят в гранулоциты палочкоядерного и сегментоядерного типа.
Палочкоядерные имеют ядро в виде колбаски. Ядро сужается и получается сегментоядерный гранулоцит. Все формы до миелоцита в норме можно обнаружить только в костном мозге, а палочки и сегменты находятся как в нем, так и в крови.
Стоит затронуть такие клетки, как моноциты. Начальной единицей является монобласт, который переходит в промоноцит, а затем и в моноцит. Зачем нужны моноциты полностью не ясно. Есть предположение наличия некой связи с гранулоцитами на генетическом уровне.
Клетки-макрофаги получаются при дальнейшей дифференцировке с образованием неровностей на их поверхности. Макрофаги связаны со многими клетками и имеют огромное количество функций:
- удаляют продукты распада
- являются звеном иммунитета
- необходимы в свертывании крови
- участвуют в обмене веществ
- стимулируют некоторые процессы
И конечно же, стоит упомянуть о лимфоцитах. В ходе своего преобразования лимфоциты проходят стадию клеток предшественниц Т и В лимфоцитов. Они заполняют селезенку, лимфоузлы. Такие клетки проходят дифференцировку от предшественников Т и В лимфоцитов до зрелых клеток. Регуляция этого процесса контролируется цитокинами.
Производство тромбоцитов
Начальным этапом производства тромбоцитов является стволовая клетка гемопоэтического типа. Основными этапами ее преобразований является:
- перевод клетки в нужное русло дифференцировки
- деление клеток путем митоза
- увеличение плоидности клетки
- рост цитоплазмы
- выход тромбоцитов в русло
На ранних стадиях тромбоцитопоэза основным регулятором служит тромбопоэтин. Сами тромбоциты активно участвуют в свертывании крови и регулируют спазм сосудов.
Вот так, пройдя множество преобразований, стволовая клетка становится одной из клеток кровяного русла.
Контроль гемоцитопоэза
Гемоцитопоэз объединяет процессы, связанные с преобразованием различных клеток в зрелые элементы крови. Так обеспечивается естественное сокращение лишнего количества форменных элементов. Полипотентные стволовые клетки самостоятельно проходят регенерацию. Они могут образовываться вне органов кроветворения. При стандартной дифференциации полипотентные клетки, сосредоточенные в костном мозге, способствуют зарождению зрелых элементов крови. Это:
- базофилы;
- эритроциты;
- различные типы лимфоцитов;
- эозинофилы;
- нейтрофилы.
К ним относят:
- попадание инфекции в организм;
- механические повреждения и другие факторы, способствующие потере определенного количества крови;
- адаптация к условиям высокогорья.
Регуляция гемопоэза
Кроветворение регулируется:
- факторами роста, обеспечивающими пролиферацию и дифференцировку СКК и последующих стадий их развития,
- факторами транскрипции, влияющими на экспрессию генов, определяющих направление дифференцировки гемопоэтических клеток,
- витаминами, гормонами.
Факторы роста включают колониестимулирующие факторы (КСФ), интерлейкины и ингибирующие факторы. Они являются гликопротеинами, действующими и как циркулирующие гормоны, и как местные медиаторы, регулирующие гемопоэз и дифференцировку специфических типов клеток. Почти все факторы роста действуют на СКК, КОЕ, коммитированные и зрелые клетки. Однако отмечаются индивидуальные особенности действия этих факторов на клетки-мишени.
КСФ действуют на специфические клетки или группы клеток на различных стадиях дифференцировки. Например, фактор роста стволовых клеток влияет на пролиферацию и миграцию СКК в эмбриогенезе. В постнатальном периоде на гемопоэз оказывают влияние несколько КСФ, среди которых наиболее изучены факторы, стимулирующие развитие гранулоцитов и макрофагов (ГМ-КСФ, Г-КСФ, М-КСФ), а также интерлейкины.
Большинство указанных факторов выделено и применяется для лечения различных болезней. Для получения их используются биотехнологические методы.
Дифференцировка полипотентных клеток в унипотентные определяется действием ряда специфических факторов, поэтинов — эритропоэтинов (для эритробластов), гранулопоэтинов (для миелобластов), лимфопоэтинов (для лимфобластов), тромбопоэтинов (для мегакариобластов).
Большая часть эритропоэтина образуется в почках. Его образование регулируется содержанием в крови кислорода, которое зависит от количества циркулирующих в крови эритроцитов. Снижение числа эритроцитов и соответственно парциального давления кислорода, является сигналом для увеличения продукции эритропоэтина. Эритропоэтин действует на чувствительные к нему КОЕ-Э, стимулируя их пролиферацию и дифференцировку, что в конечном итоге приводит к повышению содержания в крови эритроцитов.
Тромбопоэтин синтезируется в печени, стимулирует пролиферацию КОЕ-МГЦ, их дифференцировку и образование тромбоцитов.
Ингибирующие факторы дают противоположный эффект, т.е. тормозят гемопоэз; их недостаток может быть одной из причин лейкемии, характеризующейся значительным увеличением числа лейкоцитов в крови. Выделен ингибирующий лейкемию фактор (ЛИФ), который тормозит пролиферацию и дифференцировку моноцитов-макрофагов.
Витамины необходимы для стимуляции пролиферации и дифференцировки гемопоэтических клеток. Витамин В12 поступает с пищей и соединяется с внутренним фактором (Касла), который синтезируется париетальными клетками желудка. Образуемый при этом комплекс, в присутствии ионов Са2+, соединяется с рецепторами эпителиоцитов подвздошной кишки и всасывается. При всасывании в эпителиоциты поступает лишь витамин В12, а внутренний фактор освобождается. Витамин В12 поступает с кровью в костный мозг, где влияет на гемопоэз, и в печень, где может депонироваться. Нарушение процесса всасывания при различных заболеваниях желудочно-кишечного тракта может служить причиной дефицита витамина В12 и нарушений в гемопоэзе.
Некоторые термины из практической медицины:
- анемия (син. малокровие) — состояние, характеризующееся снижением содержания гемоглобина в единице объема крови, чаще при одновременном уменьшении количества эритроцитов;
- анемия ахрестическая — общее название анемий, развивающихся вследствие неспособности эритробластов костного мозга использовать какие-либо антианемические факторы (цианокобаламин, фолиевую кислоту, железо и др.) при их нормальном поступлении в организм;
- хлороз ранний (син.: бледная немочь, хлороз ювенильный) — железодефицитная анемия у девушек в период полового созревания, проявляющаяся алебастровой бледностью кожи с зеленоватым оттенком, извращением вкуса, олигоменореей;
- хлороз поздний (син. анемия железодефицитная эссенциальная) — железодефицитная анемия у женщин в возрасте старше 30 лет, обычно связанная с маточными или другими кровотечениями, проявляющаяся извращением вкуса и обоняния, признаками атрофии слизистой оболочки полости рта и пищевода, выпадением волос, искривлением ногтей, позже — выраженными признаками анемии;
Регуляция кроветворения
Адекватный и быстрый ответ системы кроветворения на вновь возникающие потребности организма в клетках крови обеспечивают цитокины.
В норме регуляция гемопоэза осуществляется непосредственным влиянием микроокружения и гуморальными факторами, обладающими активирующим или угнетающим действием. Эти факторы получили название цитокины. Они позволяют обеспечивать адекватный и быстрый ответ системы кроветворения на вновь возникающие потребности организма в клетках крови. К цитокинам активирующего типа относятся:
- факторы роста (колониестимулирующие);
- эритропоэтины;
- фактор стволовых клеток;
- интерлейкины и др.
Угнетают клеточную активность и кроветворение следующие субстанции:
- фактор некроза опухоли;
- интерферон-гамма;
- лейкоз-ингибирующий фактор и др.
При этом подавление роста одного вида клеток может приводить к усиленной дифференцировке другого.
Количество клеток в периферической крови регулируется по принципу обратной связи. Так, содержание эритроцитов в крови и насыщение их гемоглобином зависит от потребностей тканей в кислороде. Если она возрастает, то включаются не только компенсаторные механизмы (увеличение частоты дыхания и сердечных сокращений), но и стимулируется эритропоэз.
Постэмбриональный гемопоэз
Постэмбриональный гемопоэз представляет собой процесс физиологической регенерации крови, который компенсирует физиологическое разрушение дифференцированных клеток. Он подразделяется на миелопоэз и лимфопоэз.
Миелопоэз происходит в миелоидной ткани, расположенной в эпифизах трубчатых и полостях многих губчатых костей. Здесь развиваются эритроциты, гранулоциты, моноциты, тромбоциты, а также предшественники лимфоцитов. В миелоидной ткани находятся стволовые клетки крови и соединительной ткани. Предшественники лимфоцитов постепенно мигрируют и заселяют тимус, селезенку, лимфоузлы и некоторые другие органы.
Лимфопоэз происходит в лимфоидной ткани, которая имеет несколько разновидностей, представленных в тимусе, селезенке, лимфоузлах. Она выполняет функции образования T- и B-лимфоцитов и иммуноцитов (например, плазмоцитов).
Миелоидная и лимфоидная ткани являются разновидностями соединительной ткани, т.е. относятся к тканям внутренней среды. В них представлены две основные клеточные линии — клетки ретикулярной ткани и гемопоэтические клетки.
Ретикулярные, а также жировые, тучные и остеогенные клетки вместе с межклеточным веществом формируют микроокружение для гемопоэтических элементов. Структуры микроокружения и гемопоэтические клетки функционируют в неразрывной связи друг с другом. Микроокружение оказывает воздействие на дифференцировку клеток крови (при контакте с их рецепторами или путем выделения специфических факторов).
Таким образом, для миелоидной и всех разновидностей лимфоидной ткани характерно наличие стромальных и гемопоэтических элементов, образующих единое функциональное целое.
СКК относятся к самоподдерживающейся популяции клеток. Они редко делятся. Выявление СКК стало возможным при применении метода образования клеточных колоний – потомков одной стволовой клетки.
Пролиферативную активность СКК регулируют колониестимулирующие факторы (КСФ), различные виды интерлейкинов (ИЛ-3 и др.).
Каждая СКК в эксперименте или лабораторном исследовании образует одну колонию и называется колониеобразующей единицей (сокращенно КОЕ, CFU).
Исследование клеточного состава колоний позволило выявить две линии их дифференцировки.
Одна линия дает начало мультипотентной клетке — родоначальнице гранулоцитарного, эритроцитарного, моноцитарного и мегакариоцитарного рядов гемопоэза (сокращенно КОЕ-ГЭММ).
Вторая линия дает начало мультипотентной клетке — родоначальнице лимфопоэза (КОЕ-Л).
Из мультипотентных клеток дифференцируются олигопотентные (КОЕ-ГМ) и унипотентные родоначальные клетки.
Методом колониеобразования определены родоначальные унипотентные клетки для моноцитов (КОЕ-М), нейтрофильных гранулоцитов (КОЕ-Гн), эозинофилов (КОЕ-Эо), базофилов (КОЕ-Б), эритроцитов (БОЕ-Э и КОЕ-Э), мегакариоцитов (КОЕ-МГЦ), из которых образуются клетки-предшественники. В лимфопоэтическом ряду выделяют унипотентные клетки — предшественницы для B-лимфоцитов и для T-лимфоцитов. Полипотентные (плюрипотентные и мультипотентные), олигопотентные и унипотентные клетки морфологически не различаются.
Все приведенные выше стадии развития клеток составляют четыре основных класса, или компартмента, гемопоэза:
- I класс — СКК — стволовые клетки крови (плюрипотентные, полипотентные);
- II класс — КОЕ-ГЭММ и КОЕ-Л — коммитированные мультипотентные клетки (миелопоэза или лимфопоэза);
- III класс — КОЕ-М, КОЕ-Б и т.д. — коммитированные олигопотентные и унипотентные клетки;
- IV класс — клетки-предшественники (бласты, напр.: эритробласт, мегакариобласт и т.д.).
Сразу отметим, что оставшиеся два класса гемопоэза составляют созревающие клетки (V класс) и зрелые клетки крови (VI класс).
Эритропоэз у млекопитающих и человека протекает в костном мозге в особых морфофункциональных ассоциациях, получивших название эритробластических островков.
Эритробластический островок состоит из макрофага, окруженного одним или несколькими кольцами эритроидных клеток, развивающихся из унипотентной КОЕ-Э, вступившей в контакт с макрофагом. КОЕ-Э и образующиеся из нее клетки (от проэритробласта до ретикулоцита) удерживаются в контакте с макрофагом его рецепторами.
У взрослого организма потребность в эритроцитах обычно обеспечивается за счет усиленного размножения эритробластов. Но всякий раз, когда потребность организма в эритроцитах возрастает (например, при потере крови), эритробласты начинают развиваться из предшественников, а последние — из стволовых клеток.
В норме из костного мозга в кровь поступают только эритроциты и ретикулоциты.