Глава 1. общие вопросы
Содержание:
- Фокальная узловая гиперплазия (ФУГ)
- Лечение и прогноз
- Симптоматика
- Разновидности новообразования
- Диагностика
- Строение печени
- Гепатоцеллюлярная аденома (ГЦА)
- Сосуды и нервы печени
- Причины возникновения
- Связки печени
- Лечение опухоли Клацкина
- Патология структуры печени
- Паллиативная помощь
- Проекция печени на поверхность тела
- Возможные патологии
- Что такое опухоль Клацкина
Фокальная узловая гиперплазия (ФУГ)
Фокальная узловая гиперплазия (ФУГ) считается вторым (после гемангиом) наиболее распространенным доброкачественным новообразованием печени. По данным ряда авторов, ФУГ встречается у 0,9-5% населения, в 5-20% случаев может сочетаться с кистами и гемангиомами. Согласно литературным данным, ФУГ, не имея признаки опухоли, входит в группу доброкачественных гепатоцеллюлярных опухолей эпителиальной природы. Это одиночное, округлое, неинкапсулированное образование с нарушенной печеночной архитектоникой, разделенное септами, достигающими центрального рубца. Средние размеры очага – 5,7 см (от 1,5 до 12,0 см). Установлено, что ФУГ не склонна к кровоизлияниям и не имеет злокачественного потенциала. Обычно опухоль является случайной находкой при диагностических исследованиях. Узлы малых размеров, как правило, бессимптомны. Крупные опухоли могут вызывать боли в животе.
При нативном УЗИ в большинстве случаев ФУГ визуализируются с трудом, отображаясь в виде участка округлой формы с четкими контурами, изоэхогенной или незначительно гипо- или гиперэхогенной структуры. По мнению некоторых авторов, в диагностике ФУГ контрастное УЗИ является более информативной в отличие от других методов диагностики. Появление эхоконтрастных препаратов второго поколения значительно расширило возможности метода
Это позволяет дифференцировать различные типы опухолей, учитывая их характер васкуляризации, имеющего важное значение в дифференциальной диагностике очаговых образований печени. Повышенная васкуляризация опухоли в сочетании с характерным рисунком «колеса со спицами» является патогномоничным признаком ФУГ (71,4%)
При этом частота обнаружения «питающей» артерии опухоли увеличивается до 98%. Чувствительность и специфичность УЗИ с применением внутривенного контрастирования в диагностике ФУГ достигают 83 и 98% соответственно.
Гипоэхогенное образование в печени — доброкачественная фокальная нодулярная гиперплазия. В литературе описывают, что для нее характерен центральный рубец (белая стрелка).
В-режим. В IV сегменте печени, выходя на контур печени, деформируя его, визуализируется тканевой плотности гипоэхогенное, несколько неоднородное по эхоструктуре образование размерами 50 х 40 мм, неправильной формы, с четкими ровными контурами.
Лечение и прогноз
Патологии ВВ лечат с помощью медикаментов и хирургического вмешательства
Если медикаменты оказались неэффективными, то врач назначает чреспечёночную ангиопластику или тромболитическую терапию с портосистемным шунтированием в печени. Основное осложнение тромбоза ВВ – это кровоизлияние из вен пищевода, а также ишемия кишечника. Лечить эти опасные патологии нужно только хирургическим методом.
Прогноз при патологиях воротной вены зависит от степени повреждений, которые они спровоцировали. Если тромболитическая терапия при лечении острого тромбоза оказалась не совсем эффективной, то без операции не обойтись. Тромбоз с хроническим течением грозит опасными осложнениями, поэтому пациенту сначала нужно оказать первую помощь. В противном случае повышается риск летального исхода.
Таким образом, воротная вена – это важный сосуд, который собирает кровь от желудка, селезёнки, поджелудочной железы, кишечника и транспортирует её к печени. После фильтрации она вновь возвращается в венозное русло
Патологии ВВ не проходят бесследно и грозят опасными осложнениями, вплоть до смерти, поэтому важно вовремя выявить заболевание и провести грамотную терапию
Симптоматика
Опухоль ворот печени по стадиям классифицируется отдельно от остальных анатомических структур билиарного тракта:
- Стадия 0 или in situ представляет собой выраженную дисплазию внутрипротоковой слизистой, как правило. это диагностическая находка при удалении желчного пузыря;
- 1 стадия — раковые клетки не выходят за пределы стенки протока, то есть, это четко отграниченное и сугубо внутрипротоковое поражение;
- 2 стадия — распространение злокачественного процесса за пределы желчного протока, но без вовлечения близлежащих анатомических структур, то есть раковые клетки могут быть только в окружающей жировой клетчатке;
- 3 стадия — распространение рака на сосуды или метастазы не более чем в трёх лимфатических узлах ворот при любом размере первичной опухоли;
- 4 стадия — при любом размере новообразования имеются метастазы в 4 лимфоузлах или отдалённые, в том числе печеночные, метастазы.
В подавляющем большинстве случаев главное проявление холангиокарциномы желчного протока — нарушение его проходимости с развитием механической желтухи. Симптомы желтухи фактически становятся проявлением опухоли Клацкина: изменение цвета кожи и белков глаз, кожный зуд, светлый кал при темной моче и, конечно, нарастающие симптомы интоксикации с повышением температуры тела.
До появления желтушности пациента может беспокоить прогрессивно нарастающая слабость и снижение аппетита при ощущении тяжести в правом подреберье. Характерна плохая переносимость жирных, жареных и мучных блюд, в том числе подташнивание, отрыжка горьким. Возможны эпизоды спастических болей в правом подреберье в сочетании с тошнотой и рвотой, нарушение стула — чаще диарея.
До развития желтухи биохимический анализ крови может выявить повышение уровня билирубина и трансаминаз, в моче появляются желчные кислоты. Опухолевые маркеры не характерны для холангиокарцином, но возможно небольшое повышение уровня СА 19-9, отражающее любую патологию билиарного тракта.
Разновидности новообразования
Опухоли желчных протоков, формирующих разветвленный билиарный тракт, анатомически разделяют на внутрипеченочные и внепеченочные, а карцинома Клацкина всегда внепеченочная. Большинство холангиокарцином возникает в желчном пузыре, и только треть в протоках. Половину всех протоковых раков составляют опухоли Клацкина.
Опухоль Клацкина по клеточной структуре в 90% случаев состоит из трансформировавшегося железистого эпителия, частота плоскоклеточного рака — менее 5%, ещё реже в этой области встречаются саркомы и лимфомы.
По типу роста в протоке различают следующие варианты:
- Чаще всего раковые клетки распространяются внутри стенки протока, циркулярно сужая просвет без образования четко очерченной опухоли. Такие новообразования называются склерозирующими, они типичны для протокового рака внепеченочной локализации.
- Гораздо реже раковая опухоль растёт в просвет протока в виде полипа, такую форму обозначают как папиллярная. Как правило, при таком типе течение опухоли Клацкина несколько благоприятнее, потому что рядом располагающиеся анатомические структуры вовлекаются в конгломерат чуть позже, сначала опухоль оттесняет их в сторону.
- Нодулярный вариант представляет собой смесь двух предшествующих, когда конгломерат опухоли сдавливает проток, но не типичен для злокачественного поражения внепеченочных протоков.
Опухоль Клацкина рано дает метастазы в лимфатические узлы ворот.
Развитие диагностики с внедрением КТ и МРТ позволило не только раньше выявлять патологии ворот печени, но и расширило спектр паллиативных вмешательств на билиарных протоках, что потребовало унификации анатомической классификации. Задачу отчасти выполняет система Бисмут-Колетт (Вismuth-Corlette), взявшая за основу расположение ракового образования относительно места слияния правого и левого печеночного протока в общий – бифуркацию.
По классификации Бисмут-Колетт:
- рак в общем протоке обозначается как I тип, по статистике самый частый – до половины всех случаев холангиокарциномы;
- опухоль бифуркации – II тип у каждого пятого больного;
- карцинома одного долевого – III тип, в зависимости от стороны поражения добавляется литера «А» или «В»;
- двустороннее вовлечение – IV, соотнести которое с традиционной классификацией TNM не представляется возможным.
Диагностика
На первом этапе выявить новообразование ворот печени можно при обычном УЗИ брюшной полости, это общепризнанный метод скрининга билиарной патологии.
КТ точнее УЗИ «находит» патологию в области ворот и дифференцирует изменения анатомии.
Сочетание УЗИ с эндоскопией не только хорошо визуализирует зону поражения, но и позволяет выполнить биопсию новообразования. При невозможности получения образца опухолевой ткани при эндоУЗИ, через прокол брюшной стенки выполняется чреспеченочная холангиография — заполнение протока контрастным для рентгена веществом. Морфологическая верификация обязательна, особенно при невозможности проведения операции. В части случаев клеточный материал новообразования получают при диагностической лапароскопии, которая также помогает уточнить техническую возможность выполнения радикальной операции.
Для определения степени вовлечения сосудов печеночных ворот может потребоваться их ангиографическое исследование. Уточняющая диагностика распространённости ракового поражения — МРТ брюшной полости с контрастированием, в том числе контрастирование желчных протоков при МРХПГ.
Критерии 100% достоверности диагноза холангиокарциномы:
- Опухоль на УЗИ, КТ или МРТ;
- Гистологическая верификация рака;
- Исключение других раков, метастазировавших в лимфоузлы ворот печени.
Строение печени
Снаружи печень покрыта серозной оболочкой, представленной висцеральной брюшиной. Небольшой участок в задней части не покрыт брюшиной — это внебрюшинное поле. Однако, несмотря на это, можно считать, что печень расположена интраперитонеально. Под брюшиной находится тонкая плотная фиброзная оболочка (глиссонова капсула) . Со стороны ворот печени фиброзная ткань проникает в вещество органа, сопровождая кровеносные сосуды. С учетом распределения кровеносных сосудов и желчных протоков в печени выделяют (по Куино, 1957) 2 доли, 5 секторов и 8 сегментов. В долях печени разветвляются соответствующие (правая и левая) ветви воротной вены. Согласно данным Куино, границей между правой и левой долями печени является условная плоскость, проходящая по линии, соединяющей ямку желчно- го пузыря впереди и борозду нижней полой вены сзади. Н левой доле выделяют З сектора и 4 сегмента, в правой — 2 сектора и также 4 сегмента. Каждый сектор представляет собой участок печени, в который входят ветвь воротной вены второго порядка и соответствующая ей ветвь печеночной артерии, а также нервы и выходит секторальный желчный проток. Под печеночным сегментом понимают участок печеночной паренхимы, окружающий ветвь воротной вены третьего порядка, соответствующие ей ветвь печеночной артерии и желчный проток. Левый дорсальный сектор, соответствующий первому (С 1) печеночному сегменту, включает хвостатую долю и виден только на висцеральной поверхности и задней части печени. Ллевый латеральный сектор (2-й сегмент — С II) охватывает задний участок левой доли печени. Левый парамедианный сектор занимает переднюю часть левой доли печени (3-й сегмент — С III) и ее квадратную долю (4-й сегмент — С IУ) с участком паренхимы на диафрагмальной поверхности органа в виде полосы, суживающейся кзади (к борозде нижней полой вены) . Правый парамедианный сектор представляет собой печеночную паренхиму, граничащую с левой долей печени. Н этот сектор входят 5-й сегмент (С У) , лежащий кпереди, и крупный 8-й сегмент (С УIII), занимающий заднемедиальную часть правой доли печени на ее диафрагмальной поверхности. Правый латеральный сектор, соответствующий самой латеральной части правой доли печени, включает 6-й- С УI (лежит впереди) и 7-й — С УII сегменты. Последний располагается позади предыдущего и занимает заднелатеральную часть диафрагмальной поверхности правой доли печени.
По своему строению печень — сложно разветвленная трубчатая железа, выводными протоками которой являются желчные протоки. Морфофункциональной единицей печени является долька печени. Она имеет форму призмы, размер ее в поперечнике от 1,0 до 2,5 мм. В печени человека таких долек около 500 000. Между дольками имеется небольшое количество соединительной ткани, в которой располагаются междольковые протоки (желчные) , артерии и вены. Обычно междольковые артерия, вена и проток прилежат друг к другу, образуя печеночную триаду. дольки построены ив соединяющихся друг с другом печеночных пластинок («балок») в виде сдвоенных радиально направленных рядов печеночных клеток. В центре каждой дольки находится центральная вена. Внутренние концы печеночных пластинок обращены к центральной вене, наружные — к периферии дольки. Между печеночными пластинками также радиально располагаются синусоидные капилляры, несущие кровь от периферии дольки к ее центру (к центральной вене). Внутри каждой печеночной пластинки между двумя рядами печеночных клеток имеется желчный проточек (каналец), являющийся начальным звеном желчевыводящих путей. В центре дольки (возле центральной вены) желчные проточки замкнуты, а на периферии долек они впадают в желчные междольковые проточки. Последние, сливаясь друг с другом, образуют более крупные желчные протоки. В конечном итоге в печени формируются правый печеночный проток, который выходит из правой доли печени, и левый печеночный проток, выходящий из левой доли печени. В воротах печени эти два протока сливаются, образуя общий печеночный проток, длиной 4-6 см. Между листками печеночно-двенадцатиперстной связки общий желчный проток сливается с пузырным протоком, в результате чего образуется общий желчный проток.
Гепатоцеллюлярная аденома (ГЦА)
Гепатоцеллюлярная аденома (ГЦА). ГЦА считается редко встречающейся доброкачественной опухолью, происходящей из гепатоцитов. Имеются предположения о влиянии на развитие и рост опухоли пероральных контрацептивов, экзогенных андрогенов, беременности и дисбаланса эндогенных половых гормонов. Приводятся противоречивые данные по размерам аденом – указываются цифры от 1 до 19 см, составляя в среднем 5,4 см. В некоторых случаях у пациентов отмечаются множественные аденомы. Образования хорошо очерчены. Ряд авторов отмечает характерные отличительные признаки аденом – в отличие от гемангиом они не располагаются рядом с печеночными сосудами, не занимают целую долю. Течение ГЦА в большинстве случаев бессимптомное. При размерах опухоли от 5 см и более или субкапсулярным ее расположении риск кровотечения увеличивается
Авторы подчеркивают практическую важность диагностики аденомы из-за высокого риска развития кровотечения, разрыва, малигнизации и необходимости выполнения хирургического вмешательства
При УЗИ ГЦА обычно выглядит как солитарное гетерогенное образование с четкими контурами различной степени эхогенности: 20-40% аденом представляются гипоэхогенными, 30% – гиперэхогенными, что обусловлено наличием жировых включений в тканях опухоли. По мнению ряда авторов, при использовании ЦДК в ряде случаев выявляются периферические пери- и интратуморальные сосуды.
Аденома печени
Таким образом, УЗИ органов брюшной полости в настоящее время является скрининговым методом выявления опухолей и опухолеподобных процессов печени. Благодаря достаточно высокой информативности и доступности УЗИ выполняется на первом этапе диагностики при подозрении на новообразование печени. УЗИ позволяет не только выявить опухоль в печени, но и судить о ее размерах, топографии, операбельности процесса. Интраоперационное УЗИ информативно для диагностики внутрипеченочных опухолей, поскольку во время операции другие методы исследования мало применимы.
УЗИ в режиме «серой шкалы» позволяет выявить различные изменения в паренхиме. Однако в ряде случаев провести дифференциальную диагностику между диффузными заболеваниями не представляется возможным из-за схожести эхографических признаков.
Эхография в В-режиме с допплерографией сосудистой системы печени с оценкой состояния гемодинамики позволяет уточнить характер патологического процесса. Однако, несмотря на высокую специфичность (97%), чувствительность метода в выявлении опухолей печени остается достаточно низкой (60%), что позволяет отдавать предпочтение динамическим методикам РКТ или МРТ. Кроме того, по мнению отдельных исследователей, информативность диагностического заключения УЗИ, как субъективного метода исследования, зависит от опыта и квалификации врача УЗ диагностики.
Сосуды и нервы печени
В ворота печени входят собственная печеночная артерия и воротная вена. Воротная вена несет венозную кровь от желудка, тонкой и толстой кишки, поджелудочной железы и селезенки, а собственная печеночная артерия — артериальную кровь. Внутри печени артерия и воротная вена разветвляются до междольковых артерий и междольковых вен. Эти артерии и вены располагаются между дольками печени вместе с желчными междольковыми проточками. От междольковых вен внутрь долек отходят широкие внутридольковые синусоидные капилляры, залегающие между печеночными пластинками («балками») и впадающие в центральную вену. В начальные отделы синусоидных капилляров впадают артериальные капилляры, отходящие от междольковых артерий. Центральные вены печеночных долек, соединяясь между собой, образуют поддольковые (собирательные) вены, из которых в конечном итоге формируются 2-З крупные и несколько мелких печеночных вен, выходящих из печени в области борозды нижней полой вены и впадающих в нижнюю полую вену. лимфатические сосуды впадают в печеночные, чревные, правые поясничные, верхние диафрагмальные, окологрудинные лимфатические узлы. Иннервация печени осуществляется ветвями блуждающих нервов и печеночного (симпатического) сплетения.
Причины возникновения
У большинства пациентов развитию опухоли Клацкина предшествовали заболевания билиарного тракта — холангиты инфекционной, чаще всего паразитарной природы, или аутоиммунного характера. В отличии от злокачественного новообразования желчного пузыря, не найдено доказательств какой-либо связи с желчнокаменной болезнью.
Давно замечена высокая заболеваемость холангиокарциномой зараженных определенными гельминтами — печеночной двуусткой, паразитирующей в печени и поддерживающей хроническое воспаление протоков с исходом в склерозирование.
В качестве потенциального фактора риска опухоли общего желчного протока признаются воспалительные заболевания кишечника, чаще всего неспецифический язвенный колит, встречающийся у каждого двухсотого больного опухолью Клацкина.
Традиционно не исключается соучастие в злокачественной трансформации хронических гепатитов, как вирусных, так и алиментарных при злоупотреблении алкоголем, цирроза и жирового перерождения печени при ожирении. Курение сегодня признается одним из ведущих факторов риска любой злокачественной опухоли органов билиарного тракта.
Предполагается и наследственная предрасположенность, но из-за редкости заболевания достоверных доказательств этому пока не нашли.
Поскольку российская статистика учитывает все злокачественные новообразования билиарного тракта, без разделения на возникшие в протоке или желчном пузыре, по приблизительным подсчётам опухоль Клацкина ежегодно диагностируется у 1000-1200 россиян и не имеет гендерных предпочтений.
Связки печени
Печень в своем большинстве окружена брюшинным покровом, который отсутствует только на диафрагмальной поверхности задней стенки живота и в проекции жёлчного пузыря. Спускаясь с диафрагмы на одноименную поверхность печени, брюшина образует венечную связку, латеральные края которой называются правая/левая треугольные связки.
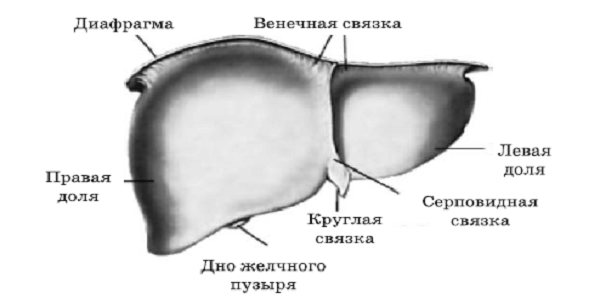
Связки печени
От висцеральной поверхности отходят следующие связки: во фронтальной плоскости – печеночно-двенадцатиперстная, которая образует в правой части передний край сальникового отверстия, к малой кривизне желудка в виде тонкой сетки – печеночно-желудочная связка (вместе обе эти связки образуют малый сальник). К правой почке отходит печеночно-почечная связка.
Лечение опухоли Клацкина
Радикальный метод лечения опухоли Клацкина — резекция части печени единым блоком с поражённым протоком. При хорошем состоянии пациента и высокой вероятности рецидива резекцию дополняют послеоперационной лучевой терапией, полугодовой профилактической химиотерапией, либо их сочетанным применением.
Более чем в 80% случаев заболевание выявляется в неоперабельной стадии. Через печеночные ворота проходят наиважнейшие для жизни органа сосуды и нервы, поэтому даже небольшой опухолевый конгломерат, особенно в совокупности с метастазированием в воротные лимфоузлы, способен серьезно нарушить их функционирование. Когда раковый инфильтрат прорастает общую печеночную артерию и воротную вену, формируя в последней тромботические массы, операция невозможна.
Противопоказание к радикальной операции — механическая желтуха вследствие внутрипротокового опухолевого стеноза, в этом случае на первом этапе проводится срочное дренирование, в том числе с установкой стента в суженый проток. После нескольких недель активной парентеральной терапии, проводимой до полной нормализации биохимических показателей крови, повторно обсуждается вопрос о возможности резекции пораженного раком участка.
В большинстве случаев при невозможности хирургического вмешательства проводится лучевая терапия на фоне приема капецитабина, после завершения облучения продолжается химиотерапия гемцитабином. При метастатической стадии возможна только длительная химиотерапия.

Тактика лечения при холангиокарциноме всегда индивидуальна и определяется мультидисциплинарным консилиумом.
Патология структуры печени
Состояние печеночной ткани можно оценить с помощью УЗИ-диагностики. Нормальные результаты исследования следующие:
- Контуры органа на всей протяженности ровные и четкие.
- Строение паренхимы гомогенное, распределение сигнала равномерное.
- Структуры ворот печени дифференцированы – четко определяется вена, артерия и желчный проток.
- Внутрипеченочные протоки расширяются к воротам печени.
- Эхосигналы гомогенны и равномерно распределены по всему органу.
Один из признаков, определяемых на эхографии – зернистость. Печеносные триады и сосуды отражают и рассеивают эхосигнал не так, как гепатоциты. За счет этой разности формируется зернистый рисунок на УЗИ.
Мелкозернистая
Такой вид на эхограмме имеет здоровый орган. Визуализируется сосудистая сеть, желчевыводящие протоки.
Качественный аппарат позволяет рассмотреть капилляры с просветом до 1 мм. Оценивается состояние воротной вены, которая должна быть в диаметре на более 12 мм. Показатель 14 мм и более позволяет судить о начале портальной гипертензии.
Изменения структуры могут наблюдаться при грубых нарушениях питания, инфекционных процессах, нездоровом образе жизни.
Крупнозернистая
Развитие патологических процессов печени, гепатиты, токсические поражения, сахарный диабет приводят к увеличению размеров печени, разрастанию соединительнотканных структур, отеку межклеточных пространств. Зернистость увеличивается. Такое состояние характеризуют как крупнозернистую структуру печени. Но это общее состояние, которое не является специфическим для конкретного заболевания.
Диффузно-неоднородная
Разрастание фиброзной ткани приводит к формированию узлов пролиферации, развитию цирроза печени. Поверхность становится бугристой, а структура диффузно-неоднородной. Данное состояние необратимо.
Любые заболевания приводят к изменениям структуры печени. Вид нарушения структуры определяется патологией.
Паллиативная помощь
Паллиативной терапии подлежит осложненное механической желтухой нарушение проходимости общего желчного протока, когда из-за раковой инфильтрации окружающих анатомических структур технически невозможно выполнить хирургическое вмешательство.
На первом этапе восстанавливается отток желчи — для декомпрессии в проток устанавливается стент или с помощью дренажа формируется обходной путь. При улучшении состояния на втором этапе возможно проведение внутрипротоковой фотодинамической терапии. Клинические исследования продемонстрировали значительное улучшение состояния и увеличение общей продолжительности жизни после нескольких сеансов фотодинамической терапии в сочетании с паллиативной химиотерапией.
ФДТ предполагает заблаговременное внутривенное введение специального фотосенсибилизующего препарата, накапливающегося в опухолевой ткани, с последующим лазерным облучением зоны поражения. Манипуляция выполняется с помощью эндо-УЗИ, что позволяет таргетное – узконаправленное воздействие с одновременным визуальным контролем эффективности процедуры. Ещё одно преимущество ФДТ – возможность многократного применения до полного уничтожения ракового конгломерата. Спектр противопоказаний для фотодинамической терапии настолько узок, что позволяет применять её у тяжелых пациентов.
У каждого второго со стентом или дренажом на фоне химиотерапии появляются симптомы обострения хронического воспаления билиарной системы или гепатита, вследствие застоя желчи, поэтому с паллиативной целью проводится активная симптоматическая терапия.
Проекция печени на поверхность тела
Печень, располагающаяся справа под диафрагмой, занимает такое положение, что ее верхняя граница по среднеключичной линии находится на уровне четвертого межреберья. От этой точки верхняя граница круто спускается вниз вправо от десятого межреберья по средней подмышечной линии; здесь верхняя и нижняя границы печени сходятся, образуя нижний край правой доли печени. Влево от уровня четвертого межреберья верхняя граница печени спускается вниз плавно. По правой окологрудинной линии верхняя граница находится на уровне пятого межреберья, по передней срединной линии пересекает основание мечевидного отростка и заканчивается слева от грудины на уровне пятого межреберья, где верхняя и нижняя границы сходятся у латерального края левой доли печени. Нижняя граница печени идет от уровня десятого межреберья справа налево по нижнему краю правой реберной дуги и пересекает левую реберную дугу на уровне присоединения левого 8 реберного хряща к 7. С верхней границей нижняя граница печени слева соединяется на уровне пятого межреберья на середине расстояния между левой среднеключичной и окологрудинной линиями. В области надчревья печень прилежит непосредственно к задней поверхности передней брюшной стенки. у старых людей нижняя граница печени находится ниже, чем у молодых, а у женщин ниже, чем у мужчин.
Возможные патологии
Чаще всего встречаются следующие патологии воротной вены:
- тромбоз;
- портальная гипертензия;
- кавернозная трансформация;
- пилефлебит.
Тромбоз ВВ
Тромбоз воротной вены представляет собою тяжелую патологию, при котором в ее просвете формируются кровяные сгустки, препятствующие ее оттоку после очищения. При отсутствии лечения диагностируется увеличение сосудистого давления. В итоге развивается портальная гипертензия.
К основным причинам формирования патологии принято относить:
- циррозное поражение печени;
- злокачественные новообразования ЖКТ;
- воспаление пупочной вены в процессе постановки катетеров младенцам;
- воспаления органов пищеварительной системы;
- травмы и хирургия селезенки, печени, желчного пузыря;
- нарушение свертываемости крови;
- инфекции.
К редким причинам развития тромбоза относят: период гестации, продолжительный прием оральных контрацептивов. Симптомами заболевания становятся: сильный болевой синдром, приступы тошноты, заканчивающиеся рвотой, диспепсические расстройства, повышение температуры тела, геморроидальные кровотечения (иногда).
Для прогрессирующей хронической формы тромбоза – при условии частичного сохранения проходимости воротной вены – типична следующая симптоматика: скопление жидкости в брюшной полости, увеличение размера селезенки, болезненность/чувство тяжести в области левого подреберья, расширение вен пищевода, что увеличивает риск развития кровотечения.
Основной способ диагностирования тромбоза – проведение УЗИ-исследования. На мониторе тромб определяется как гиперэхогенное (плотное) образование, заполняющее и венозный просвет и ветви. Тромбы небольших размеров выявляются во время эндоскопического УЗИ. Методики КТ и МРТ позволяют выявить точные причины патологии и выявить сопутствующие патологии.
Кавернозная трансформация
Патология развивается на фоне врожденных пороков формирования вен – сужения, полного/частичного отсутствия. В этом случае в области ствола воротной вены обнаруживается кавернома. Она представляет собой множество мелких сосудиков, в определенной степени компенсирующих нарушение кровообращение портальной системы.
Кавернозная трансформация, выявленная в детском возрасте, является признаком врожденного нарушения строения сосудистой системы печени. У взрослых людей кавернозное образование указывает на развитие портальной гипертензии, спровоцированной гепатитом либо циррозом.
Синдром портальной гипертензии
Портальная гипертензия – патологическое состояние, характеризующееся увеличением давления в портальной системе. Становится причиной формирования тромбов. Физиологическая норма давления в воротной вене – не выше 10 мм рт. ст. Повышение этого показателя на 2 и больше единиц становится поводом для диагностирования портальной гипертензии.
Провоцирующими патологию факторами становятся:
- цирроз печени;
- тромбоз печеночных вен;
- гепатиты различного происхождения;
- тяжелые сердечные патологии;
- нарушения обменных процессов;
- тромбы селезеночных вен и воротной вены.
Клиническая картина портальной гипертензии выглядит следующим образом: диспепсическая симптоматика; тяжесть в области левого подреберья, желтуха, снижение веса, общая слабость.
Что такое опухоль Клацкина
Опухоль Клацкина обобщённо — это рак ворот печени, а точнее — карцинома, развившаяся в желчных протоках, или холангиокарцинома.
Печеночные ворота — место вхождения внутрь органа более двух артерий с нервами, выхода наружу нескольких крупных вен, множества лимфатических сосудов и желчных протоков. Ворота небольшие по размеру — от 6 до 18 квадратных сантиметров.
Из каждой печеночной доли исходит по крупному желчному протоку, они сливаются в общий желчный проток. Опухоль Клацкина развивается либо в долевом протоке, либо в общем жёлчном протоке, протяжённость которого не превышает 5 см при несколько меньшем диаметре.
В воротах может развиться и опухоль печени, и протока или желчного пузыря, и метастазы в лимфоузлы. Все структуры взаимодействуют, поэтому при локальном новообразовании диагноз позволяет поставить только микроскопия опухоли.
Опухоль Клацкина не может развиться в ткани печени, она появляется только в слизистой оболочке протока, но быстро прорастает внутрь печени, сдавливая её сосуды и нервы, перекрывая просветы долевых желчных протоков.