Нарушения сердечного ритма
Содержание:
- Как работают кардиостимуляторы и имплантируемые кардиовертер-дефибрилляторы
- Одинаково ли проявляются нарушения ритма сердца?
- Эмбриология
- Влияние сердечной недостаточности
- Блокада правой ножки пучка Гиса — Нарушения ритма и проводимости сердца
- Подтверждение синдрома слабости синусового узла
- Причины возникновения аритмии
- Сопутствующие психические расстройства
- Диагностика СССУ
- Функции современных кардиостимуляторов
- Типы заболевания
- Хирургическое лечение
- Причины брадикардии у детей
- Формы заболевания СССУ
- Нервное питание
Как работают кардиостимуляторы и имплантируемые кардиовертер-дефибрилляторы
Кардиостимуляторы и ИКД – это маленькие электронные устройства, имплантируемые в Ваше тело. Они следят за ритмом Вашего сердца и могут синхронизировать работу его камер. Когда в нужный момент времени не происходит сокращения сердца или когда камеры сокращаются не одновременно, кардиостимуляторы и ИКД воспринимают это и посылают электрический импульс, вызывающий сокращение сердца. Эти устройства не конкурируют с естественными водителями ритма, но замещают их, когда необходимо.
Два различных ресинхронизирующих устройства могут использоваться при лечении СН:
- Специальные кардиостимуляторы с бивентрикулярным режимом стимуляции;
- Комбинированные устройства, объединяющие в себе функции и кардиостимулятора, и дефибриллятора.
Одинаково ли проявляются нарушения ритма сердца?
Все нарушения ритма и проводимости клинически проявляют себя по разному у разных пациентов. Часть больных никаких симптомов не ощущает и узнает о патологии только после планового проведения ЭКГ. Эта часть больных незначительна, так как в большинстве случаев пациенты отмечают явную симптоматику.
Так, для нарушений ритма, сопровождающихся учащенным сердцебиением (от 100 до 200 ударов в мин), особенно для пароксизмальных форм, характерно резкое внезапное начало и перебои в сердце, нехватка воздуха, болевой синдром в области грудины.
Некоторые нарушения проводимости, например пучковые блокады, ничем не проявляются и распознаются только на ЭКГ. Синоатриальная и атрио-вентрикулярная блокады первой степени протекают с незначительным урежением пульса (50-55 в мин), из-за чего клинически могут проявляться лишь незначительной слабостью и повышенной утомляемостью.
Блокады 2 и 3 степени проявляются выраженной брадикардией (меньше 30-40 в мин) и характеризуются кратковременными приступами потери сознания.
Кроме этого, любое из перечисленных состояний может сопровождаться общим тяжелым состоянием с холодным потом, с интенсивными болями в левой половине грудной клетки, снижением артериального давления, общей слабостью и с потерей сознания. Эти симптомы обусловлены нарушением сердечной гемодинамики и требуют пристального внимания со стороны врача.
Эмбриология
Формирование основных элементов П. с. с. у эмбриона начинается на стадии трубчатого сердца, в, к-ром,, по данным Венинка (А. С. G. Wenink, 1976), кроме будущего сократительного миокарда, имеются еще четыре морфологически специализированных мышечных кольца: бульбовентрикулярное, атриовентрикулярное, синоатриальное и трункобульбарное. Из этих колец в процессе петлеобразования и формирования камер сердца развиваются все компоненты П. с. с. Бульбовентрикулярное кольцо участвует в образовании атриовентрикулярного пучка и его ножек, атриовентрикулярное — в формировании атриовентрикулярного узла и пучка, синоатриальное кольцо дает начало синусно-предсердному и атриовентрикулярному узлам. Из трункобульбарного кольца формируются структуры, функционирующие только в сердце эмбрионов.
Распространенная ранее теория Молла (F. P. Mall, 1912), согласно к-рой П. с. с. представляет остаток аурикулярного канала, в настоящее время признана несостоятельной.
Синусно-предсердный узел (nodus sinuatrialis), описанный в 1906 г. Кисом и Флеком (A. Keith, М. Flack), является генератором импульсов возбуждения сердечных сокращений (см. Автоматия). Он расположен на верхней поверхности правого предсердия между устьем верхней полой вены и ушком правого предсердия. Узел всегда выявляется макроскопически. Длина его 8—26 мм, ширина 4—13 мм, толщина 1—3 мм. Связанные с узлом пучки сердечных проводящих миоцитов проводят возбуждение к миокарду различных отделов предсердий и атриовентрикулярному узлу. Выделяют пучки, направленные к верхней и нижней полым венам, задний межвенозный пучок, описанный в 1906—1907 гг. Венкебахом (К. F. Wenckebach), передний и задний межузловые пучки,, последний был описан в 1909 г. Торелем (Ch. Thorel). Пучок, проводящий возбуждение от узла к левому предсердию и устьям легочных вен, описал в 1913 г. Ю. Тандлер, а пучок, направленный к ушку левого предсердия, обнаружил в 1916 г. Бахманн (J. G. Bachmann). Размеры и положение пучков индивидуально изменчивы, они не всегда выявляются макроскопически, хотя всегда могут быть обнаружены с помощью гистологических методов исследования (см.).
Рис. 2. Макропрепарат сердца с отпрепарированной левой ножкой пучка Гиса (полость левого желудочка вскрыта): левая ножка (1) пучка Гиса разделяется на переднюю (2), две промежуточные (3) и заднюю (4) ветви.
Атриовентрикулярный узел (nodus atrioventricularis) был описан в 1906 г. Таварой (S. Tawara) и Л. Ашоффом. Он располагается в правом фиброзном треугольнике у передневерхней части устья синуса полых вен ниже прикрепления перегородочной створки трехстворчатого клапана. Атриовентрикулярный узел, так же как пучок Гиса и его ножки, всегда выявляется макроскопически (рис. 2). Форма узла чаще округлая. Длина его 3—15 мм, ширина 1—7 мм, толщина 0,5—2 мм. От узла отходит пучок Гиса, который проникает через правый фиброзный треугольник в перепончатую часть межжелудочковой перегородки, разделяясь у верхнего края ее мышечной части на левую и правую ножки. Часть пучка на протяжении от узла до начала деления на ножки называют стволом (truncus), длина его 3—20 мм. Положение пучка в межжелудочковой перегородке индивидуально изменчиво. Левая ножка (crus sinistrum) пучка Гиса длиной 5—27 мм и шириной у места отхождения от ствола 1,5—15 мм располагается под эндокардом на левой поверхности межжелудочковой перегородки и разделяется на одном уровне на 2—4 ветви (rr. cruris), которые переходят в проводящие мышечные волокна Пуркинье. Правая ножка (crus dextrum) располагается под эндокардом на правой поверхности межжелудочковой перегородки в виде одного, значительно более тонкого, чем левая ножка, ствола, от к-рого на всем протяжении отходят ветви к миокарду правого желудочка.
Описаны также добавочные проводящие тракты — пучки Кента, Джеймса, волокна Махейма, которые макроскопически не выявляются.
Влияние сердечной недостаточности
Сердечная недостаточность может оказывать следующие влияния на сердце:
- Сердечная мышца может ослабнуть и растянуться. Ослабленная мышца не может сокращаться с должной силой, что приводит к снижению кровотока в организме. Если мышца продолжает ослабевать и растягиваться, то камеры сердца могут увеличиться в размерах. В результате увеличивается давление внутри сердца и может возникнуть обратный ток крови в легкие, приводя к затруднению дыхания.
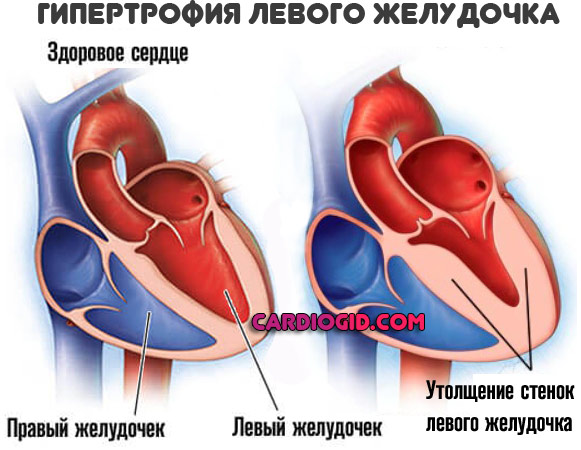
- СН также может стать причиной увеличения сердечной мышцы и нарушения ее сократимости. При увеличении сердечной мышцы уменьшаются размеры камер, снижается фракция выброса (количество крови, выбрасываемое сердцем за одно сокращение). Гипертрофия или сниженная сократимость сердечной мышцы также могут препятствовать расслаблению сердца и необходимому растяжению мышечных волокон между сокращениями, в результате чего в дальнейшем снижается объем кровотока по телу.
- В результате перечисленных изменений может нарушиться проведение импульсов от синусового узла. В результате этого желудочки могут сокращаться в разное время, что приведет к увеличению объема крови в сердце, преимущественно в левом желудочке.
- Проблемы с проведением импульсов также могут привести к нарушению ритма сердца. Оно может сокращаться медленнее, в результате чего снизится объем кровотока. Сердце также может сокращаться быстрее и/или нерегулярно. У некоторых людей с СН наблюдается комбинированное нарушение ритма сердца. Нарушение ритма может привести к увеличению нагрузки на уже ослабленное сердце.
Когда сердце не способно обеспечить нормальный кровоток, то нарушается кровоснабжение мышц, мозга и других жизненно важных органов. Кровь и другие жидкости могут застаиваться в стопах, ногах, почках и легких.
Блокада правой ножки пучка Гиса — Нарушения ритма и проводимости сердца
10.4. Нарушения внутрижелудочковой проводимости
10.4.1. Блокада правой ножки пучка Гиса (БПНПГ)
Блокада правой ножки пучка Гиса (БПНПГ) у молодых людей встречается в 0,1—0,2% случаев. С возрастом ее частота возрастает, достигая у людей старше 40 лет 0,3—0,24—4,5%. БПНПГ чаще возникает у мужчин.
При остром инфаркте миокарда БПНПГ появляется в 2—3,7% случаев и в основном при переднем инфаркте, чаще при трансмуральном. Частичная БПНПГ встречается и при заднем инфаркте миокарда.
Этиология. У молодых людей блокада правой ножки пучка Гиса часто (21— 50% случаев) доброкачественная, не связана с сердечной патологией. В остальных случаях, особенно у пожилых людей,
БПНПГ обусловлена гипертонической болезнью (60% случаев), ИБС (хотя она чаще вызывает блокаду левой ножки пучка Гиса). Реже причиной БПНПГ могут быть врожденная аномалия — недоразвитие начального сегмента правой ножки пучка Гиса; врожденные пороки сердца (дефект межпредсердной, реже межжелудочковой перегородки, стеноз устья легочной артерии); растяжение правого желудочка при тромбоэмболии легочной артерии или при обструктивных хронических заболеваниях легких (тогда чаще возникает частичная блокада правой ножки пучка Гиса); болезни Lev и Lenegre; острый инфаркт миокарда; кардиомиопатии; тупая травма грудной клетки; гиперкалиемия, прогрессирующая мышечная дистрофия; передозировка новокаинамида, хинидина, реже сердечных гликозидов; новообразования сердца; хирургические операции на сердце, например вертикальная вентрикулотомия; сифилитическая гумма.
Клиническая картина.
Могут выявляться клинические признаки органического заболевания, вызвавшего БПНПГ. Кроме того, у 1/з больных определяются некоторые изменения при аускультации: расщепление II тона, встречаемое чаще, и расщепление I тона, встречаемое реже (из-за асинхронного сокращения желудочков).
Диагностические ЭКГ-критерии. Полная БПНПГ: продолжительность комплекса #Я5>0,12 с; высокий зубец R или R’ в отведении Vi, иногда и в V2, з (перед зубцом R обычно регистрируется маленький п. В aVR отведении часто бывает глубокий зубец Q и широкий, зазубренный зубец R. В I и левых грудных отведениях обычно выявляется различной величины зубец R и широкий, зазубренный зубец S); ST и Т отклонены дискордантно от основного направления комплекса QRS. При отклонении электрической оси влево в отведении Vj регистрируются формы rR зазубренный R или qR. При отклонении электрической оси вправо в отведении V1 наблюдается форма qR.
Частичная БПНПГ: морфология комплекса QRS идентична полной БПНПГ, однако продолжительность его 0,11 с. При увеличении степени блокады продолжительность комплекса QRS увеличивается и R’ дефлексия в отведении Vi становится более высокой. Чаще (в 87% случаев) БПНПГ бывает постоянной, реже— интермиттирующей.
Лечение.
блокада правой ножки пучка Гиса в специальном лечении не нуждается. Появление БПНПГ в остром периоде инфаркта миокарда профилактической эпдокардиальной стимуляции не
требует. Если необходимо, проводят лечение основного заболевания, вызвавшего БПНПГ.
Прогноз: у молодых людей без органического заболевания сердца относительно благоприятный. Большинство авторов считают, что изолированная БПНПГ никогда не переходит в полную АВ блокаду и даже совместная находка атриовентрикулярной блокады I степени не имеет прогностического значения, так как при ЭФИ в таких случаях, как правило, находят лишь удлинение интервала А—Н, указывающее на ухудшение АВ проводимости в АВ соединении. Однако некоторые авторы указывают на редкое (1,8—6%) прогрессирование БПНПГ в АВ блокаду II или III степени.
Присоединившаяся БПНПГ на фоне гипертопической болезни или ИБС ухудшает прогноз, увеличивая летальность почти в 3 раза. Прогноз ухудшают кардиомегалия, сердечная недостаточность, удлинение интервала Н—V. Прогноз при БПНПГ всегда лучше, чем при блокаде левой ножки пучка Гиса.
На фоне острого инфаркта миокарда появившаяся полная или частичная БПИПГ не переходит, по нашим данным , в полную АВ блокаду и не ухудшает исход заболевания. Некоторые авторы при БПНПГ отмечают увеличение летальности, но только при обширном трансмуральном инфаркте миокарда с сердечной недостаточностью. На отдаленный прогноз инфаркта БПНПГ не влияет, хотя есть и противоположное мнение.
Подтверждение синдрома слабости синусового узла
Для постановки диагноза необходимо:
- Документировать, то есть доказать, что имеющиеся жалобы связаны с изменениями в сердце (медленным сокращением сердца, паузами в работе сердца, чередованиями медленного и быстрого сокращения сердца). Ведь, как уже говорилось, перечисленные признаки могут наблюдаться и при других заболеваниях.
- Отделить собственно синдром слабости синусового узла от других нарушений регуляции работы сердца.
Решить эти задачи не просто. Иногда приходится прибегать к многократным исследованиям. О них подробнее рассказано в разделе, посвященном диагностике аритмий. Далее мы коснемся только вопросов, относящихся к обсуждаемой теме.
Причины возникновения аритмии
Данное нарушение ритма появляется из-за патологических изменений, которые происходят в синусовом узле. Данное крошечное образование правого предсердия является водителем ритма первого порядка. Он генерирует электрические сигналы, что позволяет синхронизировать работу предсердий и желудочков. У здоровых людей в состоянии покоя синусовый узел генерирует 60 — 90 электрических импульсов в минуту. А в состоянии физической активности их частота растет. Например, у спортсмена, бегущего стометровку, они могут генерироваться с частотой 200 — 220 в минуту.
Проводящая система сердца
Недостаток их генерации приводит к так называемой синусовой брадикардии (снижение частоты сердечных сокращений), при которой любое физическое напряжение или эмоциональный стресс не вызывают учащения пульса. Такая неадекватная реакция сердца приводит к обморокам, головокружению и другой симптоматике. Кроме того, синдром слабости синусового узла часто сопровождается эпизодами фибрилляции предсердий (мерцательной аритмией).
Механизм возникновения данной патологии до конца непонятен. Тем не менее четко прослеживается связь СССУ с патологическими состояниями, которые приводят к образованию рубцов (фиброзу) в сердце. К ним относятся:
идиопатические дегенеративные изменения вокруг синусового узла, которые происходят в старческом возрасте;
амилоидоз;
саркоидоз;
болезнь Шагаса;
гипотиреоз;
операционная травма сердечной ткани;
инфаркт миокарда;
повышенное артериальное давление;
структурные дефекты сердца.
Помимо этого, длительный прием некоторых лекарственных средств может вызвать СССУ. Например, длительный прием следующих препаратов может привести к этой проблеме:
сердечные гликозиды (дигоксин — наиболее известный препарат из этой группы);
бета-блокаторы;
блокаторы кальциевых каналов;
антиаритмические средства (длительная лекарственная терапия какой-либо аритмии может спровоцировать появление другого вида нарушения сердечного ритма).
Сопутствующие психические расстройства
Соматоформная дисфункция сопровождается другими психическими нарушениями.
Нередко заболеванию сопутствуют фобические расстройства. Характерен страх смерти, агорафобия, канцерофобия, боязнь покраснеть.
Панические атаки – чрезвычайно частый спутник расстройства. Обуславливается состоянием сверхмощного страха и эмоционального напряжения. Характеризуется увеличением интенсивности симптомов заболевания. Нередко провоцирует развитие деперсонализации, страх потери сознания, сумасшествия, смерти.
Генерализованное тревожное расстройство вызывает сильнейшую напряженность, беспокойство, рождает опасения по поводу будущего. Помимо характерных проявлений заболевания, способствует развитию идеаторно-эмоциональных явлений. Беспокоит головокружение, слабость, ощущение дурноты. Возможно развитие дереализации, когда существующие объекты кажутся ненастоящими, а также деперсонализации. Индивид становится гиперчувствительным, остро реагирует на посторонние стимулы, ожидая опасности.
Диагностика СССУ
- Установление на ЭКГ брадикардии синусового происхождения с частотой до 40 ударов в минуту в дневное время и менее 30 уд/мин ночью может свидетельствовать о синусовой дисфункции. СА-блокада, паузы больше 3 сек, синдром тахи-брадикардии, миграция водителя ритма по предсердиям позволяют заподозрить ослабление водителя ритма.
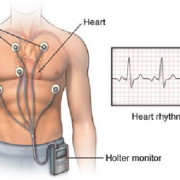
- Более информативным методом диагностики является холтеровское мониторирование ЭКГ . Оно позволяет провести анализ сердечного ритма за целые сутки и более, отследить связь нарушений с нагрузками, приемом лекарств, выявить провоцирующие факторы.
- В сложных ситуациях, когда нарушение функции СУ носит непостоянный характер, используют ЭФИ . Больному в пищевод вводится электрод, которым стимулируют предсердия до частоты 140-150 сокращений в минуту, подавляя тем самым активность естественного водителя ритма и наблюдая время восстановления функции синусного узла после прекращения стимуляции.
Функции современных кардиостимуляторов
Для полноценной работы Вашего сердца существует огромное количество параметров, режимов и алгоритмов стимуляции, для описания которых не хватит и целой книги. Расскажем только самое основное.
Самодиагностика
В современных кардиостимуляторах реализована постоянная автоматическая диагностика как работы самого стимулятора, так и работы Вашего сердца. Кардиостимулятор постоянно анализирует и записывает огромное количество различных параметров. При выявлении каких либо нарушений он может самостоятельно поменять режим стимуляции для лучшей работы Вашего сердца.
Пожизненный мониторинг сердечного ритма
Кардиостимулятор постоянно записывает все события, происходящие с Вашим сердцем и на контрольном осмотре врач может с помощью программатора посмотреть с какой частотой сокращалось Ваше сердце, как часто и каких режимах включался кардиостимулятор, даже можно посмотреть электрограмму за определенный промежуток времени, что позволяет врачу наилучшим образом скорректировать работу кардиостимулятора и лекарственную терапию.
Оценка сердечной недостаточности – немаловажная функция
Новейшая система OptiVol позволяет оценить наличие сердечной недостаточности и жидкости в легких. При этом система самостоятельно примет меры, изменит соответствующим образом режим стимуляции.
Удаленный мониторинг
Не всегда есть возможность лично явиться к врачу. В век интернета и цифровых технологий с врачом можно связаться по телефону, а информация о работе кардиостимулятора может быть передана с помощью специального устройства CareLink. Вы прикладываете его в область кардиостимулятора и через минуту Ваш врач уже знает что с Вами происходит, по телефону может дать Вам рекомендации по лечению.
Интеллектуальный подбор режима
Система Therapy Guide предлагает наиболее оптимальный режим стимуляции на основе введенных данных о пациенте. В современных кардиостимуляторах параметров очень много, в отличии от «старых» моделей, где можно менять только частоту стимуляции. Оптимальный компьютерный подбор режима сегодня важен как никогда.
Сохранение собственной проводящей системы сердца
Над этим работают все производители кардиостимуляторов в мире. Современные алгоритмы стимуляции Redused VP+, Seach AV, MVP позволяют максимально уменьшить стимуляцию сердца, тем самым сохранить собственную проводящую систему сердца.
Антитахиаритмическая функция
Конечно, кардиостимулятор предназначен для купирования брадикардии, но предупреждение и купирование тахикардии (частый пульс) имеет немаловажное значение. В сочетании с лекарственной терапией можно добиться оптимального сердечного ритма, и у Вас не будет ни бради-, ни тахикардии
Купирование фибрилляции-трепетания предсердий
Данной функцией обладают только самые современные кардиостимуляторы, которые наилучшим образом оптимизируют работу Вашего сердца и позволяют избежать неблагоприятных событий.
МРТ-совместимость
Современная медицина не представляется без точной диагностики и МРТ (магнитно-резонансная томография) все больше входит в нашу жизнь. Кардиостимулятор становится камнем преткновения. Но сегодня эта проблема уже решена: если Ваш кардиостимулятор оснащен системой SureScan, Вам можно делать МРТ любого участка тела, даже МРТ самого кардиостимулятора.
Электроды с активной фиксацией
Сводят риск смещения электрода к нулю и дают возможность имплантировать его в любой участок камеры сердца, обеспечивая наиболее физиологическое распространение электрического импульса. На конце электрода имеется «шурупчик», который вкручивается в стенку миокарда и не дает сместиться электроду.
Кардиостимулятор контролирует работу главного «мотора» Вашего организма. Чем он современней, чем больше в нем различных параметров и алгоритмов, тем лучше будет работать Ваше сердце, тем лучше будет Вам. Не стоит забывать, что кардиостимулятор имплантируется на длительный срок (около 10 лет) и чтобы его поменять, надо делать повторную операцию. Что будет с Вами завтра или через несколько лет никто не знает. Возможно, Вам потребуется МРТ, возможно разовьется сердечная недостаточность, фибрилляция предсердий или другие ситуации, с которыми не справится кардиостимулятор «старого» образца. Так может лучше сразу имплантировать самый современный кардиостимулятор, чем потом решать возникшие проблемы?
Сегодня кардиостимуляторы дают широкие возможности для лечения и мониторинга работы Вашего сердца. Выбор за Вами.
Типы заболевания
Брадикардия подразделяется на физиологическую (функциональную) и патологическую. Патологическая форма заболевания может быть острой и хронической. В зависимости от причины заболевания брадикардия делится на четыре группы:
- нейрогенная;
- органическая;
- лекарственная
- токсическая
При отсутствии причин, которые могли бы привести к замедлению сердечного ритма, специалисты говорят об идиопатической брадикардии, то есть патологии неизвестного генеза. Как правило, она выявляется у людей зрелого возраста. Это позволяет предположить связь заболевания с процессами, которыми сопровождается старение организма.
Хирургическое лечение
При тяжелой брадикардии, вызванной врожденными сердечными пороками или приобретенными заболеваниями, лечащий врач принимает решение о хирургическом лечении. Его проводят детям и взрослым при наличии показаний. В раннем детском возрасте могут устанавливаться эпикардиальные стимуляторы, эндокардиальные электроды.
Взрослым показана операция по имплантации электрокардиостимулятора. Это устройство вырабатывает электрические импульсы с нормальной частотой, что позволяет компенсировать негативные последствия замедления пульса, сохранять нормальное кровообращение.
Причины брадикардии у детей
Около 3.5% детей страдают данной патологией. Она обусловлена врожденными пороками сердца или слабостью синусового узла. В раннем возрасте брадикардия может развиться при воздействии бактериальной или вирусной инфекции. Продукты жизнедеятельности патогенов оказывают негативное влияние на работу сердца.
Генетические факторы также могут повлиять на данный процесс. В отдельную группу специалисты включают конституционально-семейную брадикардию. Склонность к снижению частоты пульса передается по наследству. Для брадикардии характерно аутосомно-доминантное наследование. Это означает, что ребенок наследует от родителей «хорошую» и «плохую» копии гена, то есть вероятность проявления заболевания составляет 50%.
К причинам брадикардии у детей и подростков специалисты относят неблагоприятную психологическую обстановку в семье, конфликты со сверстниками, чрезмерные психоэмоциональные нагрузки. Эти факторы могут усугубить развитие патологического процесса.
Формы заболевания СССУ
-
Синусовая брадикардия — ритм с частотой до 60 сокращений в минуту. Считается нормой для физически тренированных лиц, спортсменов, а также молодых людей с превалированием вагусных влияний на сердце. Кроме того, во время сна происходит физиологическое урежение ЧСС на 30%. В иных случаях брадикардия сопровождает различные заболевания.
Умеренная брадикардия может не нарушать кровообращение, однако ритм с частотой менее 40 ударов в минуту приводит к недостаточному кровоснабжению и ишемизации (дефициту кислорода) органов и тканей, нарушая этим их функцию.
Вне зависимости от причины, основа брадикардии — это нарушение способности синусного узла генерировать электрические импульсы с минутной частотой больше 60 либо некорректное их распространение по проводящей системе.
- Синоатриальная блокада.
При данном виде синусной дисфункции происходит торможение вплоть до полной остановки передачи электрической волны от водителя ритма к предсердиям. При этом наблюдается увеличение паузы между сокращениями предсердий, их временная асистолия и как следствие отсутствие своевременного сокращения желудочков, что сказывается на гемодинамике.
Механизм развития блокады бывает связан как блокированием движения импульса от источника, так и с отсутствием формирования возбуждения в самом узле.
- Остановка СУ. Синус-арест грозит внезапной остановки сердечной деятельности. Однако чаще роль источника импульсов берет на себя водитель ритма II порядка (АВ-узел), генерирующий сигналы частотой 40-60 в минуту или III порядка (пучок Гиса, волокна Пуркинье) при АВ-блокаде, частота =15-40 в мин.
Нервное питание
Частота сердечных сокращений зависит от частоты, с которой синоатриальный узел вырабатывает потенциалы действия . В состоянии покоя частота сердечных сокращений составляет от 60 до 100 ударов в минуту. Это результат активности двух наборов нервов, один из которых замедляет выработку потенциала действия (это парасимпатические нервы ), а другой — ускоряет выработку потенциала действия ( симпатические нервы ).
Симпатические нервы начинаются в грудном отделе спинного мозга (в частности, T1-T4). Эти нервы выделяют нейромедиатор, называемый норадреналином (НА) . Он связывается с рецептором на мембране узла SA, называемым бета-1-адренорецептором . Связывание NA с этим рецептором активирует G-белок (в частности, G s -протеин , S для стимуляции), который инициирует серию реакций (известных как путь цАМФ ), которые приводят к образованию молекулы, называемой циклическим аденозинмонофосфатом (цАМФ ) . Этот цАМФ связывается с каналом HCN (см. Выше). Связывание цАМФ с HCN увеличивает поток Na + и K + в клетку, ускоряя потенциал кардиостимулятора, тем самым создавая потенциалы действия с большей скоростью и увеличивая частоту сердечных сокращений. Увеличение частоты сердечных сокращений известно как положительная хронотропия .
В парасимпатические нервы , снабжающие узел SA (в частности, нервы блуждающего ) происходят в головном мозге . Эти нервы выделяют нейромедиатор, называемый ацетилхолином (ACh) . ACh связывается с рецептором, называемым мускариновым рецептором M2 , расположенным на мембране узла SA. Активация этого рецептора M2 затем активирует белок, называемый G-белком (в частности, белок G i , i для ингибирования). Активация этого G-белка блокирует путь цАМФ, уменьшая его эффекты, тем самым подавляя симпатическую активность и замедляя выработку потенциала действия. Помимо этого, G-белок также активирует калиевый канал, который позволяет K + вытекать из клетки, делая мембранный потенциал более отрицательным и замедляя потенциал кардиостимулятора, тем самым снижая скорость производства потенциала действия и, следовательно, уменьшая сердцебиение. показатель. Уменьшение частоты сердечных сокращений известно как отрицательная хронотропия .
Первая клетка, которая производит потенциал действия в узле SA, не всегда одна и та же: это называется смещением кардиостимулятора. У некоторых видов животных — например, у собак — высший сдвиг (т.е. клетка, которая производит самый быстрый потенциал действия в узле SA выше, чем раньше) обычно вызывает учащение сердечного ритма, тогда как нижний сдвиг (т.е. клетка, производящая потенциал самого быстрого действия в узле SA ниже, чем раньше) вызывает снижение частоты сердечных сокращений.