Креатинин, мочевина и цистатин с: нормы и отклонения при заболеваниях почек
Содержание:
- Когда назначается биохимический анализ крови?
- Расшифровка результатов анализа мочевины в крови
- Анализ на С-реактивный белок
- Симптомы подагры
- Профилактика
- Как и при каких условиях вырабатывается мочевина
- Последствия
- Каково клиническое течение подагрического артрита?
- Клинические признаки
- Текст подготовил
- Как проводится исследование
- Что такое билирубин, значение
- Народные рецепты
- Расшифровка
- Возможные осложнения
- Диета
- Материал для исследования
Когда назначается биохимический анализ крови?
Врач может назначить биохимический анализ крови в следующих случаях:
- в целях выявления патологии. Биохимический анализ крови может помочь установить нарушения в работе того или иного органа, даже если отсутствуют проявленные симптомы. Именно поэтому врачи рекомендуют сдавать кровь на анализ биохимии два раза в год в порядке скринингового обследования. Это позволит обнаружить заболевания на ранней стадии, что значительно облегчит их последующее лечение. Выявленные изменения химического состава свидетельствуют о неблагополучной ситуации и означают необходимость медицинского вмешательства.
- Для уточнения диагноза. Результаты биохимического анализа крови позволяют уточнить картину заболевания и являются необходимым дополнением к данным осмотра и жалобам пациента.
- В порядке наблюдения за ходом лечения и течением заболевания. С этой целью анализ биохимии назначается при заболеваниях внутренних органов (почек, печени, поджелудочной железы), авитаминозах, интоксикации организма.
Расшифровка результатов анализа мочевины в крови
Расшифровка результатов биохимического исследования сыворотки крови на уровень мочевины проводится с учетом показателей, которые отображены в таблице выше. В случае отклонения концентрации азотосодержащего вещества от установленной нормы можно судить о возможном развитии следующих патологий.
| Повышенные показатели | Сниженные показатели |
| Почечная недостаточность, находящаяся в острой или хронической форме течения. | Цирроз, а также другие заболевания печени, приводящие к тотальному разрушению ее тканей, снижению синтетической функции. |
| Стриктура мочеточника, увеличение простаты у мужчин, уролитиаз, обструкция мочевыводящих каналов. | Гипергидратация, белковая недостаточность или мальабсорбция |
Указанные заболевания чаще всех остальных болезней вызывают внезапное повышение или снижение концентрации азотосодержащего вещества в крови. В случае отклонения показателей мочевины от установленной нормы, сразу же по завершению расшифровки лабораторного заключения необходимо пройти обследование на предмет наличия вышеперечисленных патологий.
Анализ на С-реактивный белок
С-реактивный белок (СРБ) – очень чувствительный элемент анализа крови, который быстро реагирует даже на мельчайшее повреждение ткани организма. Присутствие С-реактивного белка в крови является предвестником воспаления, травмы, проникновения в организм бактерий, грибков, паразитов.
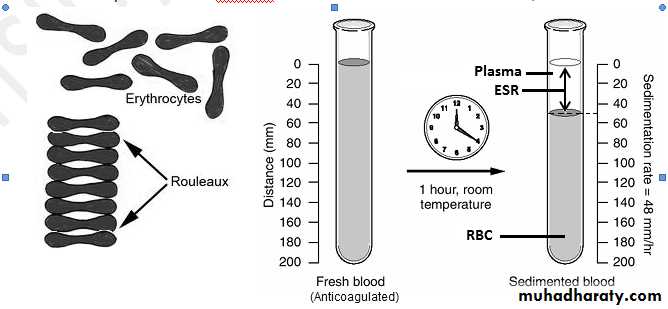
СРБ точнее показывает воспалительный процесс в организме, чем СОЭ (скорость оседания эритроцитов). В то же время С-реактивный белок быстро появляется и исчезает – быстрее, чем изменяется СОЭ.
За способность С-реактивного белка в крови появляться в самый пик заболевания его еще называют «белком острой фазы».
При переходе болезни в хроническую фазу С-реактивный белок снижается в крови, а при обострении процесса повышается вновь.
С-реактивный белок норма
С-реактивный белок производится клетками печени и в сыворотке крови содержится в минимальном количестве. Содержание СРБ в сыворотке крови не зависит от гормонов, беременности, пола, возраста.
Норма С-реактивного белка у взрослых и детей одинаковая – меньше 5 мг/ л (или 0,5 мг/ дл).
Анализ крови на С-реактивный белок берется из вены утром, натощак.
1
Анализ крови на уровень мочевой кислоты
2
анализ крови на антинуклеарные антитела
3
Исследование крови на ревматоидный фактор
Причины повышения С-реактивного белка
С-реактивный белок может быть повышен при наличии следующих заболеваний:
- ревматизм;
- острые бактериальные, грибковые, паразитарные и вирусные инфекции;
- желудочно-кишечные заболевания;
- очаговые инфекции (например, хронический тонзиллит);
- сепсис;
- ожоги;
- послеоперационные осложнения;
- инфаркт миокарда;
- бронхиальная астма с воспалением органов дыхания;
- осложненный острый панкреатит;
- менингит;
- туберкулез;
- опухоли с метастазами;
- некоторые аутоиммунные заболевания (ревматоидный артрит, системный васкулит и др.).
При малейшем воспалении в первые же 6-8 часов концентрация С-реактивного белка в крови повышается в десятки раз. Имеется прямая зависимость между тяжестью заболевания и изменением уровня СРБ. Т.е. чем выше концентрация С-реактивного белка, тем сильнее развивается воспалительный процесс.
Поэтому изменение концентрации С-реактивного белка используется для мониторинга и контроля эффективности лечения бактериальных и вирусных инфекций.
Разные причины приводят к разному повышению уровня С-реактивного белка:
- Наличие бактериальных инфекций хронического характера и некоторых системных ревматических заболеваний повышает С-реактивный белок до 10-30 мг/л. При вирусной инфекции (если нет травмы) уровень СРБ повышается незначительно. Поэтому высокие его значения указывают на наличие бактериальной инфекции.
- При подозрении на сепсис новорожденных уровень СРБ 12 мг/л и более говорит о необходимости срочной противомикробной терапии.
- При острых бактериальных инфекциях, обострении некоторых хронических заболеваний, остром инфаркте миокарда и после хирургических операциях самый высокий уровень СРБ – от 40 до 100 мг/л. При правильном лечении концентрация С-реактивного белка снижается уже в ближайшие дни, а если этого не произошло, необходимо обсудить другое антибактериальное лечение. Если за 4-6 дней лечения значение СРБ не уменьшилось, а осталось прежним и даже увеличилось, это указывает на появление осложнений (пневмония, тромбофлебит, раневой абсцесс и др.). После операции СРБ будет тем выше, чем тяжелее была операция.
- При инфаркте миокарда белок повышается через 18-36 часов после начала заболевания, через 18-20 дней снижается и к 30-40 дню приходит к норме. При стенокардии он остается в норме.
- При различных опухолях повышение уровня С-реактивного белка может служить тестом для оценки прогрессирования опухолей и рецидива заболевания.
- Тяжелые общие инфекции, ожоги, сепсис повышают С-реактивный белок до огромнейших значений: до 300 мг/л и более.
- При правильном лечении уровень С-реактивного белка снижается уже на 6-10 день.
Подготовка к ревматологическим анализам
Чтобы анализы показывали объективную информацию, необходимо придерживаться некоторых правил. Сдавать кровь нужно в утренние часы, натощак. Между взятием анализов и приемом пищи должно пройти приблизительно 12 часов. Если мучает жажда, выпейте немного воды, но не сок, чай или кофе. Необходимо исключить интенсивные физические упражнения, стрессы. Нельзя курить и употреблять спиртное.
Симптомы подагры
Первую стадию подагры описывают как гиперурикемию (повышенное содержание мочевой кислоты в крови). Гиперурикемия выявляется с помощью биохимического анализа крови. При этом в большинстве случае иных симптомов заболевания не обнаруживается. Иногда могут наблюдаться общая слабость, потливость, зуд кожи, запоры.
Собственно о подагре стоит говорить с момента начала острых подагрических атак. Спровоцировать приступ подагрического артрита могут:
-
приём алкоголя (единократное употребление значительной дозы);
-
переохлаждение;
-
травма сустава;
-
обычное ОРЗ.
В первую очередь, как правило, страдает сустав большого пальца ноги (I плюснефаланговый сустав). Типично поражение сустава только на одной ноге. Довольно часто затрагиваются другие мелкие суставы – лучезапястные или фаланги пальцев. В дальнейшем от подагрических атак могут пострадать и остальные суставы. У женщин заболевание может охватить сразу же несколько суставов уже в самом начале.
Обычно приступ подагрического артрита длится не более 5-7 дней, после чего наступает полная ремиссия (какие бы то ни было симптомы исчезают) – до следующего приступа. Такое течение подагры называют интермиттирующей («интервальной») стадией. Затем заболевание может перейти в хроническую стадию.
Приступ подагрического артрита
Приступ подагрического артрита проявляется острой болью в суставе. Довольно быстро область поражённого сустава отекает и краснеет. Цвет кожи над суставом может приобрести синюшный оттенок. Больной ощущает озноб, повышается температура, — возможно повышение до 38 °C и выше. Любое прикосновение к суставу усиливает боль, сустав полностью теряет подвижность. Боль может быть очень интенсивной и не сниматься анальгетиками.
В большинстве случаев приступ случается ночью, к утру боль обычно ослабевает. Однако в тяжелых случаях сильная боль может продолжаться до 3-х дней, потом её интенсивность медленно уменьшается.
Хроническая подагра
Если приступы подагрического артрита становятся частыми и протекают достаточно тяжело (периоды боли преобладают над периодами ремиссии), диагностируется хроническая подагра. Хроническая форма заболевания характеризуется усилением дисфункции пораженных суставов, а поскольку больной перестаёт ими пользоваться, развивается атрофия суставных мышц.
Специфическим симптомом подагры является образование тофусов. Тофус – это подкожное или внутрикожное скопление уратов (солей мочевой кислоты). Тофусы выглядят как узелки – плотные образования округлой формы. Диаметр их может варьироваться от 2-х мм до 5 см и более. Тофусы появляются обычно приблизительно через 5 лет после первого приступа подагры, медленно увеличиваясь в размерах. Однако при неблагоприятном течении их образование может идти более быстро. Типичные места, где они возникают – это пальцы рук и ног, ушные раковины, коленные и локтевые суставы, стопы, надбровные дуги. Трогать эти образования не больно. Кожа над тофусами, как правило, сухая и шероховатая, так как её кровоснабжение нарушено. Со временем в этом месте может образоваться свищ, сквозь который выделяется белая пастообразная масса (собственно ураты).
Тофусы образуются не всегда (только у 50-60% больных).
Хроническая подагра также часто становится причиной мочекаменной болезни. Ураты могут образовывать камни в почках, которые способны вызывать почечные колики, блокировать отток мочи, способствовать развитию пиелонефрита.
Профилактика
Чтобы избежать повышения мочевины в крови, необходимо внимательно следить за рационом питания, отказаться от вредных привычек, а также придерживаться следующих рекомендаций:
- не употреблять нефротоксические препараты (многие из медикаментов угнетают работу почек, например, нестероидные противовоспалительные препараты, препараты железа и т.д., после отмены которых мочевина в крови нормализуется);
- избегать использования высокобелковых диет для похудения (диета Аткинса, Дюкана, кремлевская и т.д.);
- сочетать низкокалорийную диету с употреблением алкогольных напитков;
- заниматься посильными физическими нагрузками, но избегать изнуряющих занятий спортом.
Как и при каких условиях вырабатывается мочевина
Мочевина в крови повышена (причины тревожного симптома могут быть взаимосвязаны с образом жизни человека) только в тех случаях, когда происходит ежедневное употребление пищи богатой протеинами, но при этом наблюдается сниженная работоспособность почек.
Процесс выработки биохимического соединения происходит следующим образом:
- Продукты питания, содержащие в своем составе белки растительного или животного происхождения, поступают в пищеварительный тракт.
- Под воздействием ферментов и желудочного сока происходит распад и усвоение питательных элементов еды.
- В тканях печени завершается стадия белкового обмена, в результате которой азотосодержащие продукты преобразуются в мочевину.
- Биохимическое вещество попадает в кровеносное русло, а затем проходит фильтрационный барьер почек.
- Органы выделительной системы, которые полноценно выполняют свои функции, выводят мочевину из организма вместе с уриной.
В составе мочевины содержится не менее 46% азота. Люди, которые длительное время не употребляют белков животного происхождения, либо же умышленно ограничивают себя в приеме пищи, содержащей большое количество протеина, имеют низкие показатели мочевины. При этом данный результат характерен, как для состава сыворотки крови, так и для урины.
Последствия
Отсутствие медикаментозного лечения при повышенном уровне мочевины может привести к острой или хронической почечной недостаточности. При этом показатель содержания мочевины может достигнуть 100-200 ммоль/литр при норме 1,4-8,3 ммоль/л.
Развитие почечной недостаточности приводит к тому, что в крови повышается мочевина и другие химические продукты метаболизма, поскольку отсутствует фильтрация плазмы крови почками. При этом наблюдаются сопутствующие осложнения, а именно:
- артериальная гипертензия (стойкое повышение давления);
- протеинурия (белок в моче);
- гиперелипидемия (повышенный уровень липидов в крови);
- гиперпаратиреоз (гиперактивность паращитовидной железы);
- проблемы со свертываемостью крови;
- нарушение электролитного баланса.
Каково клиническое течение подагрического артрита?
Для подагрического артрита характерно стадийное течение патологического процесса:
- I стадия. Бессимптомная гиперурикемия.
- II стадия. Острый подагрический артрит.
- III стадия. Период между приступами.
- IV стадия. Хроническая тофусная подагра. Кристаллы моноурата натрия откладываются подкожно, в синовиальные ткани или в субхондральной зоне костей.
I стадия. Бессимптомная, асимптоматическая гиперурикемия (продромальный период: диспептические явления, подавленное настроение, полиурия). Может быть психоэмоциональное возбуждение. Образно об этом писал T. Sydenham: «яркое солнце перед бурей».
Характерно:
1) повышение содержания мочевой кислоты в крови при отсутствии клинических признаков отложения кристаллов (то есть без артрита, тофусов, нефропатии или уратных камней). Гиперурикемия повышает риск развития подагры и нефролитиаза, однако во многих случаях подобных поражений нет.
2. Гиперурикозурия. Значительно повышает риск формирования уратных камней у лиц с экскрецией мочевой кислоты более 1000 мг/сут. У таких больных возможна острая обструкция мочевых путей — одна из форм острой почечной недостаточности, часто сопровождающая противоопухолевую химиотерапию. Другие лекарственные препараты, способствующие гиперурикозурии, представлены в табл. 7.
Высокая нагрузка пуриновыми основаниями приводит к внезапному повышению содержания мочевой кислоты в крови с последующим выпадением кристаллов в мочевых путях.
II стадия. Острый подагрический артрит. Поражение суставов является основным клиническим признаком подагры. Оно может проявляться острым подагрическим артритом, интермиттирующим артритом или хроническим артритом с отложением периартикулярных тофусов. Чаще эта первая манифестная форма подагры. Приступ развивается у большинства больных (80–90%) среднего или старческого возраста с предшествующей асимптоматической гиперурикемией в течение 20–30 лет.
Самостоятельное затихание воспалительного процесса в суставе при подагре определяется способностью фагоцитов переваривать кристаллы и выделять ряд антивоспалительных факторов, в частности трансформирующий фактор роста бета.
III стадия. Межприступный период. Выделение межприступного периода имеет принципиальное практическое значение, поскольку систематическое лечение в этот период позволяет не только предотвратить дальнейшее прогрессирование болезни, но и будет способствовать обратному развитию уже образовавшихся тофусов. Наступает после окончания первого приступа и может прерваться следующей острой атакой. Но и в межприступный период подагра продолжает прогрессировать. Лишь примерно у 7% больных после первого эпизода подагры повторных атак не отмечают.
Некоторые больные подагрой испытывают приступ лишь однажды в жизни, другие — многократно. Хотя между первым и вторым приступом иногда проходит 40 лет и более, у 75% больных второй приступ наблюдается в течение 2 лет после первого. В межприступный период боль в суставах не отмечается. Однако у 62% повторные приступы возникают в течение первого года болезни.
В типичных случаях в межприступный период пациенты не предъявляют жалоб, но если больной не получает лечения, то каждая последующая атака протекает тяжелее и межприступный период сокращается.
IV стадия (финальная). Хроническая тофусная подагра. При хронической подагре симптомы в пораженных суставах полностью не устраняются. Для этой формы заболевания характерно появление тофусов, хроническое течение артрита. Хронический подагрический артрит развивается в тех суставах, в которых ранее отмечалось несколько острых подагрических приступов, проходивших без остаточных явлений
Такое течение заболевания наблюдается как результат недостаточного лечения острых приступов или, что особенно важно, тактики лечения в межприступный период
Клинические признаки
- Анорексия, подавленность
- Рвота обусловленная гиперацидным гастритом, полидипсия, полиурия. Гингивит с язвами на кончике языка. Анемичные слизистые оболочки. Наблюдается вторичный гиперпаратиреоз с размягчением костей лицевого черепа.
- Констипация, обезвоживание
- При пальпации можно обнаружить изменение размеров почек, чаще всего они уменьшены, если ХПН вызвана амилоидозом, гидронефрозом, опухолями – наблюдается увеличение почек.
- Уремическая энцефалопатия: кома, тремор, эпилептиформные припадки, тетеания.
- Аритмия брадикардия. Повышение артериального давления, гипертрофия левой половины сердца. Ацидоз вызывает углубление дыхания.
- Иммунная депрессия, обызвествление мягких тканей, нарушение свертываемости крови, резистентность к инсулину (повышение уровня глюкозы в крови), нарушение работы поджелудочной железы (гиперамилаземия). Истончение волоса, плохое качество шерсти.
- У кошек с терминальной стадией ХПН наблюдается летаргия.
Диагностика
ХПН можно диагностировать болезнь животного по клиническим симптомам, но они могут быть и неспецефическими, т.к. подавленность, летаргия, отсутствие аппетита и потеря веса наблюдаются при многих заболеваниях. Для подтверждения диагноза требуются лабораторные исследования. В нашей клинике мы используем чаще всего биохимический и клинический анализы крови и анализ мочи, во многих случаях проводим ультразвуковое исследование почек.
Определяются повышенный уровень мочевины, азота мочевины и креатинина. Определение креатинина в крови имеет большее значение, чем определение мочевины, т.к уровень креатинина не подвержен влиянию диеты или уровню расщепления белков.
Также можно определять скорость клубочковой фильтрации: определяют объем и концентрацию креатинина в моче за сутки и коррелируют с уровнем креатинина в сыворотке крови.
Симптомы отсутствия аппетита наблюдаются при уровне мочевины более 25 ммольл, при содержании мочевины 40 ммольл (норма 5-10 ммольл) у животного будут наблюдаться сильное угнетенение и анорексия.
Недостаточное выведение огранического фосфора приводит к подъему его уровня в крови, в то время как уровень кальция падает (при ХПН средней тяжести уровень фосора не более 2,1 ммольл, при тяжелой форме ХНП более 3,2 ммольл).
Высвобождение кальция из костей при высоком уровне фосфора приводит к минерализации мягких тканей. У большинства кошек с ХПН наблюдается гипонатриемия иили гипокалиемия, гипоальбуминемия, гиперамилаземия. Нерегеративная анемия, гипокалиемия. Изостенурия, плотность мочи 1008 и ниже.
Преобладает следующая картина: нерегенеративная анемия вызванная снижением производства почками эритропоэтина и уменьшением срока жизни циркулирующих эритроцитов, лейкоцитоз с лимфопенией и тромбопенией.
Изостенурия (осмоляронть обычно ниже 1015), рН изменяется в кислую сторону, протеинурия, неактивный мочевой осадок, редко глюкозурия.
Повышение эхогенности почечной паренхимы, размытость границ коркового и медиального слоя, уменьшение размеров почек.
Определяется уменьшение размеров почек менее 2,5 кратной длины тела второго поясничного позвонка (L-2). Если наблюдается явный гиперпаратиреодизм, то видно снижение плотности костей, особенно верхней челюсти и кальцификация мягких тканей.
Дифференциальный диагноз
Дифференцируют от острой почечной недостаточности (ОПН), преренальной и постренальной уремии.
При ОПН отсутствует анемия, полиурия и полидипсия, уменьшение почек, зато присутствуют анамнестические признаки экстраренального основного заболевания.
Гломерулонефрит сочетается с сильной протеинурией, при этом размеры почек в норме, тенденции к отекам.
При пиелонефрите в анализе мочи активный мочевой осадок, пиурия. Почки могут быть неправильной формы, расширение лоханки и мочеточников на УЗИ. Лейкоцитоз крови.
От полидипсии без задержки мочевины, Diabetes mellitus, Dibetes isipidus centralis and renalis, психогенной тяги к питью.
При гистопатологическом исследовании почек (биопсия) при ОПН наблюдается:
- острый некроз канальцев
- острое воспаление
При ХПН:
- значительная часть нормальной паренхимы заменена фиброзной тканью,
- обширная атрофия канальцев,
- кальцификация базальных мембран,
- хроническое воспаление (хронический интерстициальный нефрит),
- гломерулосклероз
Текст подготовил
Котов Максим Анатольевич, главный врач центра КТ «Ами», кандидат медицинских наук, стаж 19 лет
Список источников
- Campbell B., De Silva D., Macleod M., Coutts S., Schwamm L., Davis S., Donnan G. Ischaemic stroke, 2019.
- Bouchez L., Sztajzel R., Vargas M. CT imaging selection in acute stroke, 2016.
- Kamalian S., Lev M., Stroke Imaging, 2019.
- Котов М.А. Возможности компьютерной томографии в прогнозировании летального исхода инсульта / Дневник казанской медицинской школы. — 2017. — №. 2. — С. 76-80.
- Котов М.А. Показатели и значение интракраниального анатомического резерва, у пациентов с острым нарушением мозгового кровообращения / Журнал научных статей Здоровье и образование в XXI веке.Т. 18, № 2., 2016. — С. 229-233.
- Котов М.А. Лучевые предикторы исходов ишемического инсульта / Дневник казанской медицинской школы. — 2018. — №. 2. – С. 86-89.
- Котов М.А. Предикторы раннего летального исхода острого нарушения мозгового кровообращения, выявляемые при компьютерной томографии / Материалы VIII Научно-практической конференции Поленовские чтения, Российский нейрохирургический журнал им. проф. А.Л. Поленова, специальный выпуск. — 2018, — Т.Х, С. 129.
- Котов М.А. Возможности компьютерной томографии в оценке риска развития острого нарушения мозгового кровообращения / Вестник Северо-Западного государственного медицинского университета им. И.И. Мечникова. 2017. Т. 9. № 4. — С. 35-38.
- Kotov M.A. Brain dislocation morphometry at neurology and neurosurgery from the standpoint of evidence-based medicine / Global Science and Innovation // Materials of the V international scientific conference. — Chicago, 2015. — Р. 207-212.
Как проводится исследование
Для получения данных о МСН в анализе крови осуществляется забор крови из вены. В редких случаях возможно использование капилляров пальца (сейчас практически не используется, так как отличается меньшей точностью и информативностью). Данная процедура выполняется медицинской сестрой или работником лаборатории, имеющим соответствующее образование и лицензию на осуществление этой деятельности. Её длительность составляет не более 5 минут и сопровождается незначительной болезненностью и дискомфортом в месте прокола. Однако неприятные ощущения быстро исчезают, а на месте прокола может остаться небольшой синяк. Лицам, испытывающим страх от вида крови, настоятельно рекомендуется отвернуться и не смотреть на руку до окончания процедуры. Но для предотвращения потери сознания и быстрого введения в чувство в кабинете всегда присутствует ватный диск и нашатырь. Забор крови проводится в несколько последовательных стадий:
- Наложение резинового или тканевого жгута с фиксаторами на предплечье пациента, который должен немного поработать кулаков (несколько раз сжать и разжать руку для лучшего наполнения сосудов).
- Лаборант или медсестра выбирает наиболее подходящую вену и обрабатывает кожу спиртовым тампоном.
- Введение иглы в вену, по которой кровь поступает в шприц или специальную пробирку. Зачастую, набирается не более 5 мл.
- Извлечение иглы и накладывание на место прокола ватки, смоченной в спирте.
Для предотвращения появления кровоподтёков или формирования синяков, пациента просят на несколько минут прижать предплечье к плечу. На этом процедура заканчивается и медицинский работник подписывает пробирку, после чего полученный материал размещается в анализаторе. Его использование даёт возможность в автоматическом режиме подсчитать все виды кровяных клеток, включая эритроциты. Полученные данные отправляются лечащему врачу, после чего начинается расшифровка анализа крови МСН.
Что такое билирубин, значение
Молекула билирубина представляет из себя 4 пиррольных кольца, соединенных между собой. Молекулярная масса молекулы — 548,68. Чистый билирубин — это труднорастворимое кристаллическое вещество.
Являясь продуктом распада эритроцитов, билирубин токсичен. Его непрямая форма постоянно образуется в тканях и крови и не выводится из организма. Печень перерабатывает ядовитое вещество, преобразует его в прямую форму, растворимую в воде. Прямая форма выводится с калом или мочой, окрашивая их в коричневый цвет.
Сумма фракций может давать в целом нормальное значение общего билирубина, но часто бывает, что первичный билирубин повышен, а связанный – ниже нормы. Такое фракционное соотношение наблюдается при начальных формах ферментной недостаточности печени и угрозе чрезмерного накопления токсичного непрямого билирубина в тканях.
Народные рецепты
Использование лекарственных трав разрешается при повышении уровня мочевины, не связанном с заболеваниями. При диагностировании патологии их применение нужно обговаривать с врачом.
Удалить излишки мочевины поможет мочегонный отвар на основе толокнянки, створок фасоли и кукурузных рылец. Травы берут в равных пропорциях и 40 г смеси заливают 1 л воды, кипят 15 мин. Затем процеживают, выпивают за сутки в 6 приемов. С этой целью можно использовать отвар из корней шиповника. Берут 2-4 шт. размером 5-10 см, заливают 1 л воды и кипятят 30 мин.

Превышение нормы карбамида в крови может быть признаком патологий, поэтому при наличии любых симптомов, указывающих на появление проблемы, стоит обратиться к врачу. Только диагностика поможет избежать осложнений, в том числе летального исхода.
Расшифровка
Исходя из полученных результатов, специалистом определяются дальнейшие действия по лечению и профилактике повышенного уровня мочевины. Показатели нормы разнятся в зависимости от возраста, пола, а также исходя из дополнительных особенностей организма.
Средние значения описаны в следующей таблице:
| Категория | Показатель, ммоль/л |
| Новорожденные и недоношенные дети | 1,7-5,0 |
| Дети до 3 лет | 1,8,-6,3 |
| Дети до 14 лет | 1,9-6,7 |
| Взрослые люди до 60 лет | 2,5-7,5 |
| Взрослые люди после 60 лет | 2,8-8,3 |
Обычно норма уровня мочевины в крови у мужчин выше, чем у женщин, — в среднем 3,7-7,5 ммоль/л. Эта особенность обусловлена наличием частых физических нагрузок, объемом мышечной массы и преобладанием в рационе питания большого количества жирных сортов мяса. Значительное отклонение показателя нередко указывает на проблемы в предстательной железе, что при отсутствии лечения может привести к эректильной дисфункции и раку простаты.
Уровень нормы количества мочевины в крови у женщин составляет 2,5-7,0 ммоль/л. Однако в период беременности показатель может отличаться от среднего значения.
Возможные осложнения
Избыточная концентрация азотосодержащего соединения, находящегося в составе крови, должна быть удалена в максимально кратчайшие сроки.
Отсутствие медикаментозного или другого метода терапии, способно привести к развитию следующих осложнений:
- тяжелая форма уремии, которая предусматривает накопление мочевины до критических приделов и наступление комы;
- общая интоксикация организма;
- развитие сердечной недостаточности;
- возникновение гипертонического криза;
- ишемическая болезнь сердца;
- гепатит или цирроз печени;
- пожизненная зависимость от аппарата искусственная почка с необходимостью прохождения диализного очищения крови не реже 1 раза в неделю;
- наступление летального исхода.
В таком случае можно рассчитывать на экстренное принятие мер, направленных на снижение уровня азотосодержащих веществ без существенного нарушения обменных процессов в организме. В целом же нарушение нормальных показателей мочевины в составе сыворотки крови – это явный симптом тяжелых заболеваний внутренних органов, либо же системной дисфункции тканей почек и печени.
Диета

Повышенная мочевина в крови может нормализоваться после коррекции питания: из рациона исключаются белки животного происхождения, способствующие активному образованию мочевины.
С целью понижения уровня мочевины используется лечебная диета 7 стол, которая является щадящей для органов выделительной системы.
Основные принципы лечебной диеты для снижения уровня мочевины следующие:
- принимать пищу 4-5 раз в день небольшими порциями, чтобы избегать нагрузки на печень и почки;
- пить большое количество жидкости (1,5-2 литра в день);
- полностью исключить белок животного происхождения (мясо, колбасные изделия, субродукты и блюда из них, консервы из мяса и рыбы, копчености, мясные и рыбные бульоны);
- исключить шоколад и какао, крепкий чай и кофе, сдобную выпечку, алкогольные напитки;
- ограничить употребление продукции кисломолочного производства (нежирный сыр, творог, сметана, йогурт) и яиц (до 2 в неделю);
- ограниченно можно употреблять растительное и сливочное масло, галетную выпечку.
Рацион должен состоять из сложных углеводов, при переваривании которых не выделяется аммиак и не образовывается повышенная мочевина, а именно:
- крупы (гречневая, овсяная, рисовая, пшеничная и т.д.);
- свежие и термически обработанные овощи (морковь, лук, кабачки, капуста, картофель);
- фрукты и ягоды, орехи, сухофрукты.
Материал для исследования
Для обнаружения специфических антител к токсоплазме производится забор крови из вены, особой подготовки процедура не требует. Для проведения ПЦР-реакции подходит любой биологический материал – кровь, слюна, образцы тканей, другие биологические жидкости (ликвор, моча).
Если возникает потребность в диагностике токсоплазмоза у плода возможен забор крови из пупочного канатика. Процедура назначается редко потому что связана с высоким риском осложнений и преждевременного прерывания беременности. Более щадящая методика – взятие на анализ околоплодной жидкости путем пункции. Эти методики применяют в случае, когда результаты специфических анализов беременной с подозрением на токсоплазмоз не дают достаточной ясности диагноза.
Показания к применению различных лабораторных исследований и особенности интерпретации результатов у разных категорий обследуемых
В зависимости от категории пациента (возрастной группы, группы риска) показано применения различных наборов методик диагностики. Особенно важен правильный выбор диагностических методов в случае подозрений на токсоплазмоз у беременных женщин.