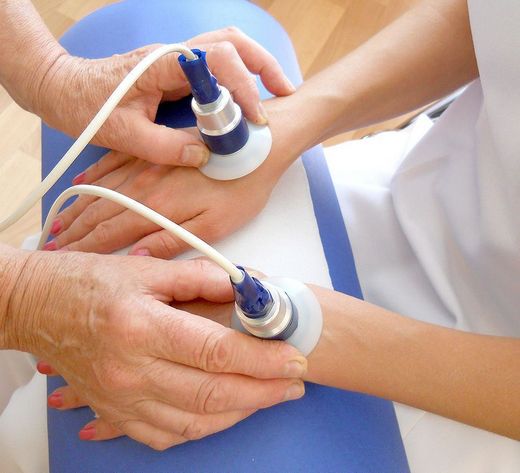
Лучевая терапия
Содержание:
- 2.Проблемы с кожей, выпадение волос, проблемы с пищеварительной системой
- Особенности применения лучевой терапии в онкологии при разных видах рака
- Трехмерная конформная лучевая терапия (3D-CRT)
- Самая вредная диагностика
- Что является источником энергии для наружной ЛТ?
- Как проводят лучевое лечение?
- Текст подготовил
- Какие существуют новые подходы к ЛТ?
- Диагностика рака на III стадии
- Как радиоактивное ионизирующее излучение воздействует на организм человека?
- Наружное облучение
- Реабилитация
- Осложнения лучевой терапии у детей
2.Проблемы с кожей, выпадение волос, проблемы с пищеварительной системой
Лучевая терапия и проблемы с кожей
Еще один побочный эффект лучевой терапии проявляется в том, что кожа выглядит как после долгого пребывания на солнце. Она может быть красной и загорелой. Иногда появляются отеки и волдыри, сухость, шелушение и зуд. Кожа может «слезать», как будто вы обгорели на солнце.
Поэтому для облегчения состояния кожи после лучевой терапии нужно придерживаться нескольких рекомендаций:
- Не носите тесную одежду в области, на которую воздействует излучение;
- Не трите кожу, используйте мягкое мыло и теплую воду для умывания;
- Не прикладывайте ничего холодного или горячего на пострадавшие участки без рекомендации врача;
- Проконсультируйтесь с врачом, прежде чем использовать любые мази, масла, крема или лосьоны;
- Избегайте солнца. Носите закрытую одежду и спросите у врача о том, какие солнцезащитные средства лучше использовать;
- Если лучевая терапия используется для лечения рака молочных желез, не носите бюстгальтер. Или выбирайте хлопчатобумажные модели без косточек;
- Не бинтуйте пораженные участки, если этого не рекомендовал врач.
Раздражение кожи уменьшается через несколько недель после окончания лучевой терапии. Но даже после выздоровления кожа может приобрести более темный оттенок. И в любом случае после лучевой терапии нужно защищать кожу от солнца в течение года после курса лечения.
Выпадение волос при лучевой терапии
Выпадение волос после лучевой терапии бывает у тех пациентов, которые получают излучение в области головы. Если волосы выпадают, это обычно происходит внезапно и в большом количестве Волосы могут выпадать целыми прядями. В большинстве случаев после завершения курса лучевой терапии волосы начинают расти снова. Но они могут быть тоньше или иметь другую структуру.
Один из способов минимизировать потерю волос после лучевой терапии – это укоротить их до начала лечения, чтобы вес волос стал меньше. Если волосы выпадают, обязательно нужно носить головной убор, чтобы защитить голову от солнечных лучей.
Проблемы с пищеварительной системой
Лучевая терапия в зоне головы, шеи или органов пищеварительной системы может стать причиной потери аппетита
Но даже в этом случае важно правильно питаться, чтобы сохранить силы и здоровье
Вот несколько рекомендаций:
- Ешьте маленькими порциями по пять-шесть раз в день. Это лучше, чем большая тарелка еды три раза в день.
- Попробуйте какие-то новые продукты или наоборот, привычные и любимые блюда. Возможно, они вызовут аппетит.
- Перекусы помогут поддержать силы, когда вы голодны и не имеете возможности полноценно поесть.
Особенности применения лучевой терапии в онкологии при разных видах рака
При раке шейки матки
Метод входит в схемы лечения начальных стадий рака и комплексной терапии объемных новообразований, применяется после удаления шейки матки для профилактики рецидивов, используется для угнетения роста неоперабельных опухолей.
При раке предстательной железы (простаты)
Курс ЛТ назначают на ранних стадиях заболевания при отказе больного от операции или невозможности ее проведения, на поздних стадиях в комплексе с гормонотерапией, после удаления простаты для профилактики рецидивов. Возможные последствия при раке предстательной железы – осложнения в виде синдрома раздраженного кишечника, цистита, снижения потенции, сужения (стриктуры) мочеиспускательного канала – при использовании современных методов и соблюдении рекомендаций врача встречаются редко.
При раке молочной железы
Облучение применяется при комплексном подходе на всех стадиях болезни. Особенно высока профилактическая роль ЛТ после операции с сохранением молочной железы (частичной резекции). Новообразования молочной железы чувствительны к увеличению дозы облучения, поэтому в последнее время приоритет отдается стереотаксическим вариантам.
При раке легкого
Назначение радиотерапии в предоперационный период увеличивает шанс удаления малооперабельных раковых опухолей (например, новообразования в верхушке легкого), в постоперационный – снижает риск возникновения местных рецидивов.
При опухолях головного мозга (в просторечие рака мозга)
С появлением в онкологии методов высокоточной лучевой терапии появилась возможность разрушать злокачественные новообразования головного мозга при невозможности хирургического вмешательства, высоком риске осложнений или отказе больного от традиционной операции. В настоящее время активно применяются такие виды, как кибер-нож и гамма-нож;
Трехмерная конформная лучевая терапия (3D-CRT)
Традиционная и самая оптимальная терапия при раке молочной железы, которую предложат в нашей стране — трехмерная конформная лучевая терапия. Конечно, есть и другие виды лучевой терапии, например, технологии IMRT, IGRT, но для них требуется очень дорогое высокоточное оборудование, и не каждая клиника этим оборудованием оснащена, да и специалистов, работающих с этим оборудованием, у нас в стране не так много. Трехмерная (3D) конформная лучевая терапия представляет собой точное составление плана лечения с компьютерной поддержкой на основании современных методов визуализационной диагностики, которое позволяет проводить максимально точное (конформное) облучение целевой области с обеспечением максимально щадящего воздействия на здоровые прилегающие ткани и органы, находящиеся в зоне риска.
Возможность трехмерного моделирования позволяет достаточно точно определить объемы и взаиморасположение опухоли, а также окружающих нормальных органов и тканей. Поэтому для составления плана лучевой терапии на компьютерном томографе получают трехмерное изображение пациента. При этом тело пациента находится в том же положении, что и при самой лучевой терапии
Это очень важно и обеспечивается благодаря использованию специальных систем для контроля размещения и сохранения положения тела на обоих устройствах (КТ и ускоритель). При помощи фиксирующих приспособлений, таких как доски для фиксации рук, подколенники, маски, вакуумные матрасы и т. д., положение пациента на столе фиксируется и может быть в любое время воспроизведено.
На основании этой плановой компьютерной томографии и/или магнитно-резонансной томографии (МРТ) лечащий радиотерапевт в индивидуальном порядке на всех КТ-уровнях определяет для каждого пациента целевой объем облучения и органы, находящиеся в зоне риска и требующие максимальной защиты. Так создается трехмерное изображение области, на которой будет проведена лучевая терапия.
Эксперт медицинской физики при помощи специального программного обеспечения рассчитывает индивидуальный план лечения, в котором строго соблюдаются международные стандарты предельно допустимых доз облучения на здоровые органы. Каждое поле облучения ограничено так называемыми коллиматорами и, следовательно, имеет индивидуальные границы. Также медицинские физики определяют основные параметры облучения: вид и энергию излучения, направления и количество пучков. В конечном счете цель лечения заключается в том, чтобы облучить всю опухоль той дозой облучения, которая необходима для достижения оптимального эффекта, и как можно лучше защитить окружающие здоровые органы и ткани от негативного воздействия. Мастерство врача как раз и состоит в том, чтобы подобрать максимально эффективное (радикальное, как часто говорят) лечение с наименьшими, по возможности, осложнениями. Как правило, готовый план лучевой терапии оценивается не одним врачом, а группой специалистов и, при необходимости, корректируется.
Вот так выглядит план лучевой терапии при лечении молочной железы:
Красным цветом оконтурен объем опухоли. Другими цветами — окружающие критические органы риска. В левой части экрана — распределение дозы в трех проекциях. В правом нижнем углу — гистограмма доза-объем, по которой мы оцениваем распределение дозы. В остальных двух окнах — 3-Д-реконструкция срезов компьютерной томографии пациентки.
Самая вредная диагностика
Для сравнения «вредности» различных видов рентгеновских исследований можно воспользоваться средними показателями эффективных доз, приведённых в таблице. Это данные из методических рекомендаций № 0100/1659-07-26, утверждённых Роспотребнадзором в 2007 году. С каждым годом техника совершенствуется и дозовую нагрузку во время исследований удаётся постепенно уменьшать. Возможно, в клиниках, оборудованных новыми аппаратами, вы получите меньшую дозу облучения.
| Часть тела | Доза мЗв/процедуру |
| Флюорография цифровая | |
| Грудная клетка | 0,05 |
| Органы малого таза | 0,3 |
| Рентгенограмма цифровая | |
| Грудная клетка | 0,03 |
| Конечности | 0,01 |
| Кишечник | 0,2 |
| Почки | 0,1 |
| Органы малого таза | 0,1 |
| Зубы, челюсть | 0,02 |
| Молочная железа | 0,05 |
| Рентгеноскопия | |
| Кишечник | 12 |
| Пищевод, желудок | 3,5 |
| Компьютерная томография (КТ) | |
| Грудная клетка | 11 |
| Конечности | 0,1 |
| Шея | 5,0 |
| Органы малого таза | 9,5 |
| Голова | 2,0 |
| Зубы, челюсть | 0,05 |
Очевидно, что самую высокую лучевую нагрузку можно получить при прохождении рентгеноскопии и компьютерной томографии. В первом случае это связано с длительностью исследования. Рентгеноскопия обычно проводится в течение нескольких минут, а простой рентгеновский снимок делается за доли секунды. Поэтому при динамичном исследовании вы облучаетесь сильнее.
КТ предполагает серию снимков: чем больше срезов — тем выше нагрузка, это плата за высокое качество получаемой картинки.
Ещё выше доза облучения при сцинтиграфии, так как в организм вводятся радиоактивные элементы. Вы можете прочитать подробнее о том, чем отличаются флюорография, рентгенография и другие лучевые методы исследования.
Что является источником энергии для наружной ЛТ?
Источниками являются радиоактивные изотопы йода-125, -131, стронция-89, фосфора, палладия, цезия, иридия, фосфата или кобальта. Другие изотопы еще исследуются.
Энергия может поступать следующим образом:
- Рентгеновские или гамма-лучи, оба являются формами электромагнитного излучения. Хотя они образуются по-разному, везде используются фотоны.
- Рентгеновские лучи создаются аппаратами – линейными ускорителями. В зависимости от количества энергии в рентгеновских лучах, последние могут быть использованы для уничтожения раковых клеток на поверхности тела (низкий энергетический уровень) и в более глубоких структурах (высокий энергетический уровень). По сравнению с другими типами излучения, рентгеновские лучи могут облучать достаточно большую область.
- Гамма-лучи продуцируются, когда изотопы некоторых элементов (иридий и кобальт 60) высвобождают лучистую энергию при распаде. Каждый элемент распадается с определенной скоростью и каждый высвобождает разное количество энергии, что определяет глубину проникновения в тело (гамма-излучение, образующееся при распаде кобальта-60, используется в лечении «гамма-нож»).
- Пучки частиц: используются субатомные частицы вместо фотонов. Пучки частиц генерируются линейными ускорителями, синхротронами и циклотронами. При таком лечении используются электроны, генерируемые рентгеновскими трубками, нейтроны, генерируемые радиоактивными элементами и специальным оборудованием. Тяжелые ионы (протоны и гелий), ?-мезоны (пионы) – малые отрицательно заряженные частицы, генерируемые ускорителями и системой магнитов. В отличие от рентгеновских и гамма-лучей, пучки частиц проникают в ткани неглубоко, поэтому часто используются в лечении поверхностных опухолей и опухолей под кожей.
Терапия пучками протонов это тип терапии пучками частиц. Протоны располагают энергией в очень маленькой области – максимуме Брэгга. Его можно использовать для лечения опухоли высокими дозами при малом повреждении соседних нормальных тканей. Пока применяется редко. Сейчас ведутся исследования по использованию такой терапии в лечении интраокулярной меланомы, ретинобластомы, рабдомиосаркомы, рака простаты, легкого и мозга.
Как проводят лучевое лечение?
Лучевая терапия – это широкий арсенал методов, которые можно разделить на две большие группы: внешнюю и внутреннюю (брахиотерапию). В первом случае излучение генерируют специальным аппаратом, который двигается возле проблемной зоны и под разными углами посылает лучи в опухоль. Пациент при этом лежит неподвижно на столе в той позе, которую выбрали на этапе планирования. Время воздействия может быть разным. В среднем один сеанс занимает 10-30 минут. В большинстве случаев пациенту назначают несколько таких процедур. Через некоторое время курс повторяют. Если целью радиотерапии является обезболивание, то ее могут провести однократно.
Сама процедура абсолютно безболезненная, но вызывает у некоторых людей беспокойство. Комнаты для проведения облучения оборудованы аудиоаппаратурой. С ее помощью пациент может сообщить врачам о любой проблеме или просто поговорить, чтобы расслабиться. Сами доктора в это время находятся в соседней комнате.
Брахиотерапия предполагает облучение опухоли радиоактивными веществами, которые вводят непосредственно в новообразование или соседние ткани. Она имеет две разновидности: временная и постоянная. При временном варианте радиоактивные препараты находятся внутри специального катетера, который на некоторое время вводят в опухоль, а затем удаляют. Для постоянной брахиотерапии используют крохотный имплантат, который помещают непосредственно в опухоль, где из него постепенно высвобождаются радиоактивные вещества. Со временем они заканчиваются, а зерно имплантата остается в организме на всю жизнь, не причиняя никаких неудобств.
Текст подготовил
Котов Максим Анатольевич, главный врач центра КТ «Ами», кандидат медицинских наук, стаж 19 лет
Список источников
- Campbell B., De Silva D., Macleod M., Coutts S., Schwamm L., Davis S., Donnan G. Ischaemic stroke, 2019.
- Bouchez L., Sztajzel R., Vargas M. CT imaging selection in acute stroke, 2016.
- Kamalian S., Lev M., Stroke Imaging, 2019.
- Котов М.А. Возможности компьютерной томографии в прогнозировании летального исхода инсульта / Дневник казанской медицинской школы. — 2017. — №. 2. — С. 76-80.
- Котов М.А. Показатели и значение интракраниального анатомического резерва, у пациентов с острым нарушением мозгового кровообращения / Журнал научных статей Здоровье и образование в XXI веке.Т. 18, № 2., 2016. — С. 229-233.
- Котов М.А. Лучевые предикторы исходов ишемического инсульта / Дневник казанской медицинской школы. – 2018. – №. 2. – С. 86-89.
- Котов М.А. Предикторы раннего летального исхода острого нарушения мозгового кровообращения, выявляемые при компьютерной томографии / Материалы VIII Научно-практической конференции Поленовские чтения, Российский нейрохирургический журнал им. проф. А.Л. Поленова, специальный выпуск. — 2018, -Т.Х, С. 129.
- Котов М.А. Возможности компьютерной томографии в оценке риска развития острого нарушения мозгового кровообращения / Вестник Северо-Западного государственного медицинского университета им. И.И. Мечникова. 2017. Т. 9. № 4. — С. 35-38.
- Kotov M.A. Brain dislocation morphometry at neurology and neurosurgery from the standpoint of evidence-based medicine / Global Science and Innovation // Materials of the V international scientific conference. — Chicago, 2015. – Р. 207-212.
Какие существуют новые подходы к ЛТ?
Изучается совместное применение гипертермии (высокие температуры) совместно с ЛТ. Ученые выяснили, что при таком сочетании опухоль лучше «отвечает» на лечение.
Также исследователи изучают антитела, меченные радиоактивными метками, для доставки излучения непосредственно в опухоль (радиоиммуннотерапия). Антитела это высоко специфичные белки, образующиеся в организме в ответ на появление антигенов (чужеродные вещества, распознающиеся иммунной системой). У некоторых опухолевых клеток есть специфические антигены, которые запускают продукцию опухоль-специфических антител. Большое количество этих антител может быть произведено в лаборатории, далее к ним присоединяют радиоактивные метки (radiolabeling). При введении в организм антитела ищут раковые клетки, которые разрушаются излучением. Такой подход минимизирует риск повреждения соседних здоровых тканей.
Изобретены следующие препараты: ибритумомаб тиуксетан (Zevalin) и йод-131 тоситумомаб (Bexxar), которые используются для лечения распространенной неходжкинской лимфомы взрослых. В клинических испытаниях изучается лечение подобными препаратами рака печени, легкого, мозга, простаты, щитовидной железы, груди, яичников, поджелудочной железы, колоректального рака и лейкемии. Открыты и другие препараты: гефитиниб (Iressa) и иматиниб мезилат (Gleevec).
Диагностика рака на III стадии
Для проведения диагностики рака на третьей стадии врач тщательно собирает анамнез болезни со слов больного, ориентируясь в первую очередь на его жалобы.
Далее, исходя из данных анамнеза и физикального осмотра (внешний осмотр и пальпация), назначается план обследования. Основными пунктами этого плана являются следующие методы обследования:
- Непрямая и Прямая ларингоскопия (фиброларингоскопия). Последняя позволяет произвести осмотр всех отделов гортани с максимальной четкостью. Введение инструмента в гортань не причиняет какого-либо вреда больному, позволяя выполнить высококачественную фото и видеосьёмку.
- Во время фиброларингоскопии выполняется биопсия опухоли и полученные образцы тканей отправляются на гистологическое (включая иммуногистохимическое) и цитологическое исследования для постановки морфологического диагноза (чтобы понять какого строения опухоль, степень ее дифференцировки)
- УЗИ шеи и органов брюшной полости ( для исключения или определения метастазов, их локализации и размеров)
- Рентгенография органов грудной клетки ( для исключения метастазов в легких)
Современная медицина дает возможность не только диагностировать заболевание, но и выявить его особенности.
Если полученных данных врачу недостаточно для постановки диагноза или определения операбельности, то прибегают к назначению уточняющих или дополнительных методов диагностики:
- компьютерная томография (КТ) шеи, органов грудной клетки
- магнитно-резонансная томография (МРТ) шеи, органов грудной клетки, органов брюшной полости)
- Радиоизотопное исследование костей скелета
- определение связи опухоли с наличием HPV (ВПЧ) – инфекции (ВПЧ – Вирус Папилломы Человека)
- молекулярно-генетическая диагностика опухолевой ткани ( при планировании таргетной или иммунной терапии)
Вышеперечисленные диагностические методы необходимы для правильной постановки диагноза и назначения соответствующего лечения.
Как радиоактивное ионизирующее излучение воздействует на организм человека?
Радиоактивное излучение запускает механизм выработки свободных радикалов. Их избыток при низком антиоксидантом (защитном) статусе организма приводит к разрушению клеточных компонентов, в том числе к деструкции и сокращению теломеров — концевых участков молекул ДНК. Также процессу окисления подвержены липиды и белки мембран.
В норме организм человека легко переносит диагностические мероприятия и самостоятельно восстанавливается — дополнительно ничего предпринимать не нужно. Вслед за окислительными процессами, вызванными свободными радикалами, начинается восстановление, и ресурсов организма для этого достаточно.
В конце ХХ — начале XXI века был открыт фермент теломеразы (активен в половых, стволовых и онкологических клетках). За его открытие Э. Блэк-Бёрн, К. Грейдер и Дж. Шостак были удостоены Нобелевской премии в 2009 году. Теломераза отвечает за «удлинение» теломеров, это значит что их разрушение нельзя считать необратимым. Однако ученые заметили и другую закономерность: рак и рост онкологической опухоли возможен тогда, когда молекулы ДНК существенно укорочены и повреждены, при этом фермент теломеразы пребывает в активном состоянии. Это своеобразный «сбой» генетической программы, который приводит к опасным последствиям.
В целом, среднестатистический здоровый организм взрослого человека в состоянии восстановиться после облучения, равного 50-100 мЗв в год. При большем систематическом воздействии радиации развивается лучевая болезнь.
Наружное облучение
В практике нейроонкологии в подавляющем большинстве случаев используется наружное облучение, которое проводится при помощи гаммаустановок, в которых в качестве источника излучения применяется радиоактивный изотоп (кобальт-60 или цезий-137) , или линейных ускорителей электронов, в которых жесткое рентгеновское излучение генерируется при ударении ускоренных электронов об мишень, или ускорителей протонов. Принципиальной разницы в противоопухолевом эффекте излучения из этих источников нет, но излучение линейного ускорителя и протонный пучок позволяют получать более отграниченный от окружающих тканей очаг воздействия, что снижает риск радиационного повреждения здоровых тканей.
Наружное облучение может проводиться фракционно, с использованием разовых фракций от 1,5 до 5 Гр в течение достаточно длительного периода (до 1,5 месяцев). Это проводится с расчетом того, что при каждой очередной фракции облучения повреждаются клетки опухоли, находящиеся в радиочувствительной фазе своего жизненного цикла. При этом суммарная доза облучения доводится до 45-78 Гр.. В части случаев, при небольших размерах опухоли используется радиохирургия: наружное облучение в разовой дозе 15-25 Гр. Это массивное облучение по противоопухолевому эффекту равнозначно фракционированному, но оно применимо только в небольшом числе случаев.
Реабилитация
После облучения человеческому организму требуется продолжительный период восстановления. Процесс реабилитации – это заключительный и очень важный этап лучевой терапии. Он может проходить дома или в тяжелых случаях в условиях стационара. Врач дает подробные рекомендации, обязательно включающие в себя индивидуальный рацион, распорядок дня, легкие физические нагрузки, режим трудовой деятельности и отдыха. Особо отмечается необходимость беречь облученные участки кожи от прямых солнечных лучей не менее года. Неукоснительное выполнение больным всех рекомендаций поможет его организму восстановить нормальную работу всех своих систем. По окончании периода реабилитации пациенту назначаются даты обязательных контрольных осмотров. При ухудшении состояния больному следует обратиться к лечащему врачу, не дожидаясь установленных сроков. Примерный перечень таких симптомов:
- повышение температуры тела, кашель;
- боль, не проходящая в течение 3–5 дней;
- потеря аппетита, тошнота, понос;
- появление опухоли или отека в области облучения;
- появление кожных высыпаний.
Последние исследования результатов лечения онкологических больных с применением лучевой терапии показывают, что с 90-х годов прошлого века риск осложнений значительно снизился благодаря применению качественно новых целенаправленных техник облучения. Все больше и больше пациентов, прошедших лучевую терапию, полностью восстанавливаются и сохраняют здоровье на долгие годы.
Осложнения лучевой терапии у детей
Лучевое лечение является одним из важных компонентов лечения злокачественных опухолей у детей. Специфика детского организма и развитие опухолевого процесса определяют ряд особенностей проведения лучевой терапии и возникновения побочных реакций и осложнений.
Лучевой метод как самостоятельный редко используется у детей. Обычно облучение применяется в следующих случаях:
- Предоперационное облучение с целью уменьшения размеров опухоли.
- Послеоперационное облучение, направленное на уничтожение оставшихся опухолевых клеток после операции или при неполном (нерадикальном) удалении опухоли.
- Сочетание лучевой терапии с химиотерапией или операцией.
Подавляющее число злокачественных опухолей у детей являются высоко чувствительными к облучению.
К ним относятся: нефробластома (опухоль Вилмса), нейробластома, неходжкинская лимфома (лимфосаркома), рабдомиосаркома, саркома Юинга, болезнь Ходжкина (лимфоранулематоз).
Вместе с тем, чувствительность одной и той же опухоли у разных больных к лучевой терапии неодинакова. Это зависит от характера роста опухоли, ее размеров, длительности существования, сопутствующих заболеваний и других факторов.
Проведение лучевой терапии затруднено у маленьких детей в связи с необходимостью неподвижности больного во время облучения. Облучение в таких случаях проводится во время сна, как естественного, так и вызванного применением специальных средств.
Учитывая высокую чувствительность детей, особенно детей младшего возраста, к радиации, большой объем облучаемых тканей, тяжесть состояния ребенка, можно ожидать появление побочных эффектов. Лучевая терапия нередко сопровождается тошнотой и рвотой (при облучении живота и других областей), как проявление общей лучевой реакции.
Побочным проявлением местного воздействия облучения могут быть облысение, поражение слизистой оболочки полости рта (стоматит), расстройства кишечника в виде жидкого стула, особенно у детей младшего возраста.
Нередко наблюдаются другие побочные реакции общего характера (потеря аппетита, нарушение сна) и ухудшение показателей крови (снижение числа лейкоцитов и эритроцитов).
При достижении значительной суммарной дозы облучения возможны выраженные местные кожные реакции (покраснение, мокнутие, зуд, боль).
Химиопрепараты дактиномицин, и адриамицин усиливают поражение кожи и слизистых оболочек; циклофосфамид в сочетании с облучением нередко приводит к циститу (воспалению мочевого пузыря), а адриамицин при облучении средостения усиливает кардиотоксичность (повреждение сердечной мышцы).
Из поздних осложнений лучевой терапии следует отметить атрофию кожи, подкожной клетчатки и мягких тканей, запустевание лимфатических сосудов с развитием отеков, замедление роста и деформация костей, укорочение облученной конечности, асимметрия отдельных участков тела, остеопороз (разрежение костной ткани) и патологические переломы.
Возможно также появление рубцовых изменений в легких, поражение сердечной мышцы, катаракты и пр. Тяжелым последствием лучевой терапии через несколько лет (2-10 и более лет) является развитие второй злокачественной опухоли.